Mytoksantron: mode d'emploi du médicament, structure, Contre-
Lorsque ATH:
L01DB07
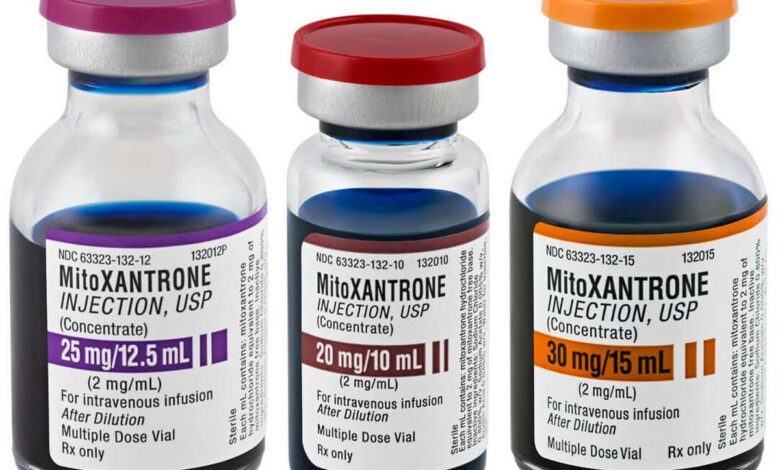
Mytoksantron – Caractéristique
Le chlorhydrate de mitoxantrone est un dérivé synthétique de l'anthracycline..
Mytoksantron – Action pharmacologique
Antitumorale, immunosuppresseur.
Mytoksantron – Demande
Cancer mammaire (avec des métastases régionales ou éloignées); cancer du foie, ovaire, prostate (incl. gormonalnoustoychivy stade IV avec la douleur); non-hodgkinien; myéloïde aiguë, promyélocytaire, monoblastnыy la leucémie; adultes de erythromyelosis (l'inefficacité des moyens traditionnels), ascite rakovyi.
Mytoksantron – Contre-
Hypersensibilité, intrathécale, grossesse, lactation.
Mytoksantron – Restrictions applicables
Évaluation du rapport bénéfice-risque dans les cas suivants: leucopénie, pancytopénie, Lourd circule comorbidités, dysfonction et / ou des reins foie, goutte, permettre vetryanaya, zona, avant cytotoxique ou une radiothérapie, les personnes âgées ou l'âge des enfants.
Mytoksantron – Grossesse et allaitement
Contre-indiqué dans la grossesse. Au moment du traitement doivent arrêter l'allaitement.
Mytoksantron – Effets secondaires
A partir du système nerveux et des organes sensoriels: mal de tête (10%), convulsions (4%), faiblesse, fatigabilité.
Système cardio-vasculaire et le sang (hématopoïèse, hémostase): insuffisance cardiaque (5%), arythmie (3%), tachycardie, douleurs à la poitrine, modifications transitoires de l'ECG, diminution de la fraction d'éjection ventriculaire, Infarctus du myocarde, gipotenziya, phlébite, saignement, leucopénie, thrombocytopénie, érythropénie.
De l'appareil digestif: perte d'appétit, nausée et vomissements (72%), diarrhée (47%), stomatite (29%), saignement gastro-intestinal (16%), douleur abdominale (15%), jaunisse (3%), ulcères dans la bouche et sur les lèvres, la fonction hépatique anormale (augmentation des niveaux de bilirubine, changement de AST, OR), constipation.
Pour la peau: alopécie (37%), lésions fongiques de la peau (15%), éruptions pétéchies / de ekhimoznye (7%), éruption, urticaire, démangeaison.
A partir du système respiratoire: symptômes pseudo-grippaux (78%), essoufflement (18%), toux (13%).
Avec le système génito-urinaire: hyperuricémie, insuffisance rénale, aménorrhée, azoospermie.
Autre: développement d'infections - 66% (incl. septicémie — 34%, les infections fongiques - 15%, pneumonie - 9%, infection des voies respiratoires supérieures - 7%), fièvre, réactions allergiques (anaphylaxie et autres.), conjonctivite (5%), irritation au site d'injection, la nécrose de la graisse sous-cutanée (en contact avec la peau et dans l'espace périvasculaire).
Mytoksantron – Coopération
Toxicité augmente et d'autres médicaments anti-tumoraux mielotoksicskie, probénécide, sulfinpirazon, la radiothérapie. Daunorubicine, doxorubicine, irradiation du médiastin augmenter le risque de cardiotoxicité. Chance augmentation de néphropathie urikozuricheskih médicaments protivopodagricakih (ajustement de la dose est nécessaire dans le traitement de l'hyperuricémie et de la goutte). AINS potentialisent les effets secondaires de sang (le risque de saignement). Affaiblit l'efficacité des vaccins de vaccination inactivé; en utilisant des vaccins, contenant des virus vivants, améliore effets viraux de réplication et secondaires de la vaccination (effet immunosuppresseur). Pharmaceutical incompatible avec la thiamine (provoquant sa destruction), l'héparine et d'autres médicaments dans la solution de perfusion ou une seringue.
Mytoksantron – Dose excessive
Symptômes: la dépression de la moelle osseuse sévère (jusqu'à 3 Soleil), agranulocytose, angine nécrotique, les infections du tube digestif, diarrhée, saignement, les manifestations de la cardiotoxicité.
Traitement: hospitalisation, la surveillance des fonctions vitales; la réduction de la dose ou l'arrêt du médicament; thérapie simptomaticheskaya; si nécessaire - la transfusion de composants sanguins, plaquettes et leucocytes masse, la nomination d'antibiotiques à large spectre.
Mytoksantron – Posologie et administration
B /, B / A, vnutrybryushynno. Le lot est individuellement. Adultes dans la leucémie pour induire une rémission - Perfusion IV en dose 12 mg / m2/jour avec 1 par 3 jour en association avec la cytarabine - 100 mg / m2/jour sous la forme d'une perfusion continue de 24 heures 1 par 7 jour. Avec peu d'effet peut mener bien sûr re-induction: mitoxantrone administré en 1 et 2 jour avec la cytarabine 1 par 5 jour la même dose. Pour maintenir la rémission - 12 mg / m2/SUT 1 et 2 journée en combinaison 100 mg / m2 cytarabine par jour, administré par voie intraveineuse pour 24 h s 1 par 5 Jour après environ 6 semaines après le cours de l'induction (deuxième cours de support est réalisée par le biais 4 semaines après la première). Lorsque le cancer de la prostate — 12 à 14 mg/m²2 1 une fois par 3 Soleil (en combinaison avec des corticostéroïdes). Lorsque le cancer du sein, le foie et le lymphome non hodgkinien - 14 mg / m2/tous les jours 3 Soleil. En thérapie combinée, la dose initiale est réduite de 2 à 4 mg/m2 par rapport à la dose de monothérapie.
Mytoksantron – Précautions
Utilisez uniquement sous surveillance médicale, avec la chimiothérapie de l'expérience. Avant et pendant le traitement (à de courts intervalles) nécessite une surveillance constante des cellules de sang périphérique, la détermination de l'hémoglobine ou de l'hématocrite, le nombre de leucocytes (global, différentiel), Plaquettaire, la détermination de la concentration d'acide urique, mener des études fonctionnelles du cœur, lumière, foie, rein. Leucopénie sévère observée pendant 10 jours (le nombre de leucocytes récupéré pour 3 Soleil), apparaît dans la mucosite 1 semaines après traitement. Si les symptômes suivants: pancytopénie, frissons, fièvre, toux ou voix rauque, douleur dans le bas du dos ou sur le côté, miction difficile ou douloureuse, saignements ou une hémorragie, selles noires, sang dans les urines ou les selles doit consulter immédiatement un médecin. Le développement de la neutropénie nécessite une surveillance attentive pour détecter à temps les signes d'infection. Devrait différer calendrier de vaccination (possible au plus tôt 3 mois ou plus récente 1 ans après la fin du dernier cycle de chimiothérapie), éviter tout contact avec des patients infectieux, ou utiliser non-événement pour la prévention des (masque, etc.). Autres membres de la famille, rester avec le patient, devrait abandonner vaccin vaccination antipoliomyélitique oral. En cas de thrombocytopénie conseillé une extrême prudence lors de l'exécution des procédures invasives, L'inspection régulière des lieux sur / dans le, peau et les muqueuses (des signes de saignement), contrôle de sang dans l'urine, vomi, Chou frisé. Les patients doivent être soigneusement rasent, manucure, brosser les dents, dentistes utilisent des fils et des cure-dents, éviter les chutes et autres blessures, boire de l'alcool et l'acide acétylsalicylique, augmenter le risque de saignement gastro-intestinal. Un traitement supplémentaire est possible après gematotoksichnosti de disparition effets. À des doses cumulées plus élevées 140 mg / m2 ou 100 mg / m2 chez les patients présentant des facteurs de risque (irradiation médiastinale, une histoire de maladie cardiaque, traitement antérieur par des anthracyclines) augmentation du risque de cardiotoxicité. Le développement de la néphropathie, en raison d'une production accrue d'acide urique, Elle peut être évitée par un apport hydrique suffisant, l'utilisation de l'allopurinol ou alcalinisation des urines. Innocuité et l'efficacité chez les enfants n'a pas été établie, il est donc nécessaire de se abstenir de nomination comme un enfant. Pendant le traitement, il est nécessaire d'utiliser des mesures contraceptives adéquates. Il faut avertir les patients du risque potentiel pour le foetus, Si au cours du traitement se pose grossesse. En cas de contact avec la peau ou les muqueuses doit être un lavage soigneux avec de l'eau (muqueuse) ou du savon et de l'eau (peau). Si vous avez extravasates cours I / injection ou l'administration de perfusion doivent arrêter et reprendre dans une autre veine.
Mytoksantron – Précautions
Après 1-2 jours peut-être la coloration bleu-vert de l'urine, dans de rares cas - coloration bleue réversible de la sclère, les veines et les tissus paravenoznyh, polonais (détachement probable de la plaque de l'ongle). Pour / dans le concentré de chlorhydrate de mitoxantrone doivent être pré-dilués 0,9% solution de chlorure de sodium ou 5% dextrose. Dissolution, la dilution et l'administration de la préparation est effectuée par le personnel médical formé à la protection (gants, masques, vêtements et autres.).
Mytoksantron – Interaction avec d'autres médicaments
| Substance active | Description de l'interaction |
| Allopurinol | FMR. Dans le contexte de la mitoxantrone (peut augmenter la concentration d'acide urique dans le sang, le risque de néphropathie développement) Il nécessite une dose accrue. |
| Busulfan | FMR. Renforce (mutuellement) manifestations toxiques (en particulier dans les poumons). |
| Daunorubicine | FMR. Augmentations (mutuellement) le risque de manifestations cardiotoxiques. |
| Doxorubicine | FMR. Augmentations (mutuellement) la probabilité d'effets secondaires, incl. cardiaque (insuffisance cardiaque, arythmie, du myocarde et analogues.). |
| Thiamine | FV. Incompatibilité pharmaceutique. |
