Mytoksantron: 薬の使用説明書, 構造, 禁忌
ときATH:
L01DB07
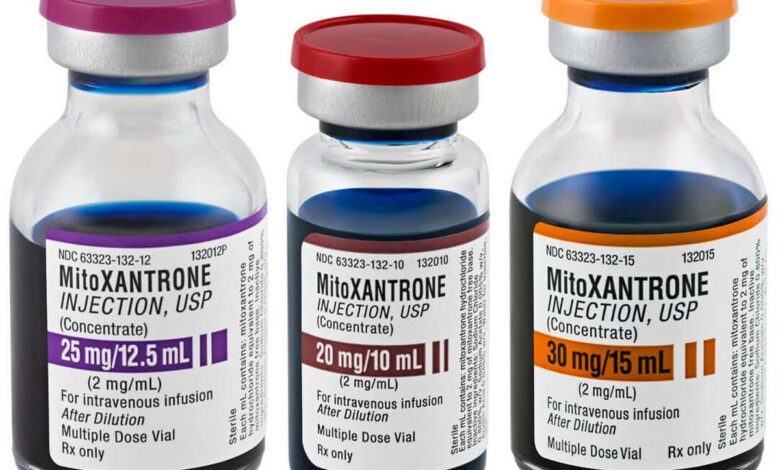
Mytoksantron – 特徴
ミトキサントロン塩酸塩は合成アントラサイクリン誘導体です.
Mytoksantron – 薬理作用
抗腫瘍, 免疫抑制性の.
Mytoksantron – アプリケーション
乳癌 (地域や遠隔転移のあります); 肝癌, 卵巣, 前立腺 (税込. 疼痛を有するgormonalnoustoychivyステージIV); 非ホジキンリンパ腫; 急性骨髄性, 前骨髄球, monoblastnыy白血病; erythromyelosis大人 (伝統的な手段の無効性), rakovyi腹水.
Mytoksantron – 禁忌
過敏症, 髄腔内の, 妊娠, 授乳.
Mytoksantron – 制限が適用されます
次の場合にリスク·ベネフィット比の評価: 白血球減少症, 汎血球減少症, 重い流れの併存疾患, 肝機能障害および/または腎臓, 痛風, vetryanayaを有効にします, 帯状疱疹, 前の細胞毒性または放射線療法, 高齢者や子供の年齢.
Mytoksantron – 妊娠中や授乳
妊娠には禁忌. 治療時に母乳を停止する必要があります.
Mytoksantron – 副作用
神経系及び感覚器官から: 頭痛の種 (10%), 痙攣 (4%), 弱点, 易疲労感.
心臓血管系および血液 (造血, 止血): 心不全 (5%), 不整脈 (3%), 頻脈, 胸痛, 過渡的ECG変化, 左室駆出率の低下, 心筋梗塞, gipotenziya, 静脈炎, 出血, 白血球減少症, 血小板減少症, 赤血球減少.
消化管から: 食欲不振, 嘔気嘔吐 (72%), 下痢 (47%), 口内炎 (29%), 胃腸出血 (16%), 腹部の痛み (15%), 黄疸 (3%), 口の中や唇に潰瘍, 異常肝機能 (ビリルビンのレベルの増加, ASTの変更, ゴールド), 便秘.
肌のための: 脱毛症 (37%), 真菌性皮膚病変 (15%), 点状出血/ ekhimoznye発疹 (7%), 発疹, じんましん, かゆみ.
呼吸器系から: インフルエンザ様症状 (78%), 息切れ (18%), 咳 (13%).
泌尿生殖器系と: 高尿酸血症, 腎不全, 無月経, 無精子症.
その他: 感染症の発症- 66% (税込. 敗血症- 34%, 真菌感染症- 15%, 肺炎 - 9%, 上気道感染症 - 7%), 発熱, アレルギー反応 (アナフィラキシーなどが挙げられます。), 結膜炎 (5%), 注射部位の刺激, 皮下脂肪の壊死 (皮膚に接触すると、血管周囲の空間へ).
Mytoksantron – 協力
毒性が増加し、他の抗腫瘍薬mielotoksicskie, プロベネシド, sulfinpirazon, 放射線療法. ダウノルビシン, ドキソルビシン, 縦隔の照射は心毒性のリスクを増加させます. protivopodagricakih薬urikozuricheskihチャンス腎症の増加 (用量調節は、高尿酸血症と痛風の治療に必要とされています). NSAIDは、血液の副作用を増強します (出血のリスク). 免疫不活化ワクチンの有効性を弱めます; ワクチンを使用して, 生ウイルスを含みます, ワクチン接種のウイルスの複製および副作用を増強 (免疫抑制効果). チアミンと互換性のない医薬品 (その破壊を引き起こします), 輸液や注射器中のヘパリンおよび他の薬剤.
Mytoksantron – 過剰摂取
症状: 重度の骨髄抑制 (までのため 3 日), 無顆粒球症, 壊死性狭心症, 消化管の感染症, 下痢, 出血, 心臓毒性の症状.
治療: 入院, 重要な機能を監視します; 減量または薬物の離脱; simptomaticheskaya療法; 必要な場合 - 血液成分の輸血, 血小板や白血球質量, 広域抗生物質の任命.
Mytoksantron – 投薬および管理
B /, B / A, vnutrybryushynno. バッチが個別にあり. 大人 白血病で寛解を誘導します -用量の静脈内注入 12 MG / M2/一日 1 上 3 シタラビンと組み合わせた日- 100 MG / M2/連続24時間の注入の形で日 1 上 7 日. ほとんど効果で再誘導コースを行うことができます: ミトキサントロンで投与 1 と 2 シタラビンとの一日 1 上 5 同じ用量日. 寛解を維持するために- 12 MG / M2/SUT 1 と 2 組み合わせた日 100 MG / M2 一日あたりのシタラビン, 中に静脈内投与 24 h s 1 上 5 約後の日 6 誘導コース週間後 (第2のコースをサポートすることを介して行われています 4 第一週間後). とき前立腺癌 -12〜14 mg / m2 1 回 3 日 (コルチコステロイドとの組み合わせで). とき乳癌, 肝臓および非ホジキンリンパ腫 - 14 MG / M2/毎日 3 日. 併用療法では、初期用量が2〜4 mg / m減少します2 単独療法の投与量と比較して.
Mytoksantron – 使用上の注意
唯一の医師の管理下で使用してください, 経験の化学療法と. 前および治療中 (短い間隔で) 末梢血液細胞の常時監視を必要とします, ヘモグロビンやヘマトクリットの決意, 白血球数 (全体的な, 差動), 血小板, 尿酸の濃度を決定します, 心臓の機能研究を実施, 光, 肝臓, 腎臓. 中に観察された重篤な白血球減少症 10 日 (白血球数はのために回収しました 3 日), 粘膜炎が内に表示されます 1 治療後数週間. 次のような症状の場合: 汎血球減少症, 寒気, 発熱, 咳や嗄声, 背中の下部または側面の痛み, 痛みを伴うまたは困難な排尿, 出血や出血, 黒い便, 尿や糞中の血液は、すぐに医師に相談してください. 好中球減少症の発症は、感染の兆候のタイムリーな検出のための注意深い監視が必要. ワクチン接種スケジュールを延期する必要があります (より前ではない可能性 3 月とアップ 1 化学療法の最後のサイクルが完了した後の年), 感染患者との接触を回避する、または予防するための非イベントを使用 (フェイスマスクなど). 他の家族, 患者と滞在, 免疫の経口ポリオワクチンを放棄する必要があります. 侵襲的処置を行う際に血小板減少症の場合には細心の注意を助言, 中/上の場所の定期検査, 皮膚や粘膜 (出血の兆候), 尿中の血液の制御, 嘔吐, ケール. 患者は慎重に剃るする必要があります, マニキュア, あなたの歯を磨きます, 歯科医はスレッドとつまようじを使用します, 転倒やその他の傷害を避けます, 飲酒とアセチルサリチル酸, 消化管出血のリスクを増加させます. 追加の治療が消失gematotoksichnosti効果の後に可能です. 上記の累積用量で 140 MG / M2 または 100 MG / M2 危険因子を有する患者における (縦隔放射線照射, 心臓病の歴史, アントラサイクリンでの前処置) 心毒性のリスク増大. 腎症発生, 尿酸の産生の増加に起因します, これは、適切な水分摂取によって防止することができます, アロプリノールまたは尿アルカリ化の使用. 子供の安全性と有効性は確立されていません, したがって、それは子供として任命を控えることが必要です. 治療中には、十分な避妊手段を使用することが必要です. これは、胎児への潜在的危険性の患者に警告する必要があります, 治療中に妊娠を発生した場合. 皮膚や粘膜に接触した場合、水でよく洗浄である必要があります (粘膜) 石鹸と水または (皮膚). あなたはI /注射または点滴投与中extravasatesを持っている場合は停止し、別の静脈に再開すべき.
Mytoksantron – 注意事項
尿の多分青緑色の着色1-2日後, まれに-強膜の可逆的な青色の染色, 静脈や組織paravenoznyh, ポリッシュ (爪甲の可能性剥離). ミトキサントロン塩酸塩濃縮物中の/ための事前希釈してください 0,9% 塩化ナトリウムの溶液又は 5% ブドウ糖. 解散, 調製物の希釈および投与は保護を訓練を受けた医療スタッフによって行われます (手袋, マスク, 衣類や他の。).
Mytoksantron – 他の薬との相互作用
| 活性物質 | 相互作用の説明 |
| アロプリノール | FMR. ミトキサントロンを背景に (血中の尿酸の濃度を増加させることができます, 腎症を発症する危険性) それは増加した投与量を必要とします. |
| ブスルファン | FMR. 強化 (相互に) 毒性症状 (特に肺の中). |
| ダウノルビシン | FMR. 増加 (相互に) 心臓毒性症状のリスク. |
| ドキソルビシン | FMR. 増加 (相互に) 副作用の可能性, 税込. 心臓の (心不全, 不整脈, 梗塞などが挙げられます。). |
| チアミン | FV. 医薬品の非互換性. |
