Mehanizam delovanja lekovite supstanci
U velika većina slučajeva,, u medicinske svrhe supstanca (Ligand) ima svoj efekat, Mora da ispuni određene komponente u telo-ciljni receptori, molekularna struktura, koji predstavljaju protein, manje nukleinske kiseline, Lipidnih ili drugim konfiguracijama, koji se nalazi unutar ili na površini ćelija, sa kojim to uradila., pokrenut lanac biohemijskih i physico-hemijskih procesa, uzrokuje određeni efekat.
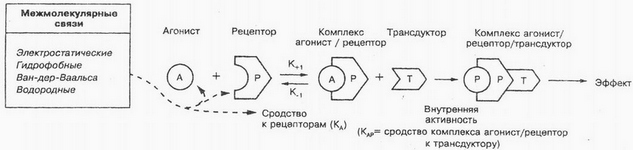
Postoje dve vrste membrana receptore-jonske kanale i receptore, G proteina u srodstvu. На пример, za adetilholina i karakterističnim za natrijum kanal slične droge. Oљljario komunicira sa kanala protein, To conformational izmene, To doprinosi Discovery Channel i prodiranje Jona natrijuma u ćeliji. Ovaj proces je osnova nervozni. Neke medicinske supstance, u interakciji sa proteina natrijum kanal, to sprečavaju otvaranje, time blokira prenos nerv preveli.
Unutrašnji deo plazma membrani ćelija sama je poravnata sa takozvane G-protein, koji obezbeđuje sinhronizacije proces lekovite supstance sa istovremenim aktivacije proteina povezanih intracellular meta. Kao što je prikazano na slici, droge molekul datoj na receptor (Н) na površinu zuba membrani, koja uzrokuje conformational promena na proteine receptora. Zahvaljujući G-protein menja svoje prostorne strukture, migrira u avionu membrane da enzima, To su u neaktivnom stanju u ćeliji. Interakcija proteina G sa enzimima (Т.) zbog njihove aktivacije (LV/R/T). Norapinefrin, dopamin i drugim ligandi u interakciji konkretno receptore, G proteina u srodstvu. Treba napomenuti, taj Oљljario mogu da ostvare interakciju ne samo sa kanala proteina, Ali sa na receptor, G proteina u srodstvu.
Za pojavljivanje interakcija između ligand i bioreceptorom bi trebalo da, da imaju komplimentarnost″û, To jest, izmedju tamo mora da bude na određene sličnosti, ili affinitet (red veličine, prostorna konfiguracija, prisustvo suprotnim optužbama i t. д.). На пример, pozitivan optužbi za spoljne ligand mora biti usklađen negativne optužbi za receptor, а неполарни радикали супстанце могу да се вежу за хидрофобне регионе рецептора.
Међу физичко-хемијским својствима лековитих супстанци, утичући на њихову интеракцију са рецепторима, потребно је одабрати величину молекула, у зависности од тога која супстанца може да ступи у интеракцију са целим рецептором или са његовом компонентом. Кинетика његовог продирања кроз биолошке мембране зависи и од величине молекула лека.. Обично се са повећањем величине молекула повећава његова флексибилност и могућност формирања ван дер Валсових веза са макромолекуларним партнером.. Штавише, важна је стереохемија молекула лека. Од, У ком изомерном облику је лек?, зависи од његове фармаколошке активности. И то се мора имати на уму: што је чвршћа конформација молекула рецептора, што је јача разлика у деловању стереоизомера.
Интеракција лековита супстанца - рецептор се врши захваљујући интермолекуларним везама. Прво, супстанца се привлачи на рецептор уз помоћ електростатичких сила., и у присуству комплементарности, формира везе са рецептором користећи физичке и физичко-хемијске интеракције (карактеристична за лекове, који се излучују из организма у непромењеном или мало измењеном облику) или хемијске интеракције (својствено везама, који пролазе кроз хемијске трансформације у телу). Најслабије ван дер Валсове силе су укључене у одређивање специфичности интеракције лековите супстанце са биохемијским реактивним системима.. Водоничне везе су укључене у процесе препознавања и фиксације супстанце (лиганд) на биоструктуре. Јонске везе настају када, када лековите супстанце садрже катјонску или ањонску групу, а супротне структуре су у биорецепторима. Често се јонске везе формирају у првим корацима фармаколошке реакције између супстанци и рецептора.. У таквим случајевима, ефекат лека је реверзибилан.. Важно је формирање координационих ковалентних веза. Уз њихово учешће, одвијају се интеракције алкилирајућих агенаса са биосупстратима., као и лекови и антидоти са металима у формирању стабилних хелатних комплекса, на пример, унитиол са арсеном или тетацин-калцијум са оловом. Дејство таквих супстанци је неповратно..
Штавише, постоји хидрофобна интеракција. Иако је енергија његових веза мала, интеракција великог броја дугих алифатских ланаца доводи до формирања стабилних система. Хидрофобне интеракције играју улогу у стабилизацији конформација биополимера и формирању биолошких мембрана.
Остаци аминокиселина у молекулу протеинског рецептора садрже поларне и неполарне групе., који одређују стварање поларних и неполарних веза између њих и лековитих супстанци. поларне групе (-ОХ, -НХ, ГУГУТАЊЕ-, -Н3В, =О) обезбеди образовање, углавном, јонске и водоничне везе. Неполарне групе (водоник, метил, циклични радикали итд.) формирају хидрофобне везе са лековима мале молекулске тежине.
Тако, интеракција лекова са специфичним рецепторима може се вршити кроз различите хемијске везе, различитом снагом. Од, приближна јачина супстанци сличних курареу са холинергичким рецепторима за електростатичке (јонски) интеракција је 5 кцал/мол, јон-дипол - 2-5 кцал/мол, дипол-дипол - 1-3 кцал/мол, водоничне везе - 2-5 кцал/мол, ван дер Валсове обвезнице - 0,5 кцал/мол, хидрофобне везе - 0,7 кцал по ЦХ2-група. Смањење јачине везе у зависности од растојања између атома за електростатичку интеракцију је р-2, јон-дипол - р-3, дипол-дипол - р-4, водоничне везе - р-4, ван дер Валсове обвезнице - р-7. Ова врста везе може бити прекинута., чиме се обезбеђује реверзибилност деловања лекова. Ковалентне везе су јаче, који обезбеђују дуго и често неповратно дејство супстанци, на пример, алкилирајући лекови против рака. Већина лекова се реверзибилно везује за рецепторе.. Kad ovo, по правилу, природа везе је веома сложена: јонски, дипол-дипол, ван дер Валса, хидрофобне и друге врсте везивања, што је у великој мери одређено комплементарношћу супстанце и рецептора и, односно, њихов степен конвергенције.
Јачина везивања супстанце за рецепторе означава се термином "афинитет". Супстанце, делујући на исте рецепторе, могу имати различите степене склоности према њима. Истовремено, супстанце већег афинитета могу да истисну супстанце са мањим афинитетом из везе са рецепторима.. Да би се утврдило стање равнотеже између "заузетих" рецептора (Др), слободних рецептора и слободне супстанце (Д) користи се константа дисоцијације ((K)Д), што је одређено следећом формулом:
(K)Д=[Д]*[Р]/[ Др]
Негативан лог КД (пРД) је показатељ афинитета. пД се често користи за карактеризацију афинитета.2, Т. то је. негативан лог ЕЦ50, (концентрација супстанце, у којој има ефекта, formiranje 50% од максималног ефекта).
Разноврсне хемијске везе интеракције и њихова неједнака снага, или се афинитет између лиганада и биорецептора објашњава сложеном структуром лекова, који садрже радикале различите реактивности и имају вишедимензионални облик, као и сложеност процеса интеракције, често се одвија у неколико фаза (фазе): формирање комплекса лек-рецептор; интрамолекуларно груписање; комплекс дисоцијације.
Тако, само супстанце са израженим афинитетом за биорецептор могу изазвати фармаколошки ефекат. Озбиљност ефекта зависи од концентрације лека и укупног броја рецептора..
Ако супстанце имају довољну интринзичну активност, називају се агонисти. Под унутрашњом активношћу подразумева се способност агониста да изазове биолошки ефекат променом конформације рецептора, Т. то је. способност лиганда да активира рецептор. Овај феномен се сматра афинитетом комплекса агонист-рецептор за трансдуктор, трансформација спољашњих сигнала у унутрашње се назива трансдукција. Интрацелуларна трансдукција сигнала лежи у основи таквих процеса, попут контракције мишићних влакана, ћелијске деобе, пролиферација, диференцијација итд.. Тренутно инсталиран, то многим супстанцама (хормони, биоактивни пептиди, Нуклеотидам, стероид, биорегулатори мале молекулске тежине итд.) ћелија има специфичне рецепторе. Као резултат интеракције ових супстанци са овим специфичним рецепторима, формирају се секундарни гласници. (посредници), који покрећу каскаду биохемијских реакција.
Постоји концепт "делимични агонисти» - лековите супстанце, да, везивање за рецепторе, не дају максималан ефекат.. Овај збуњујући феномен је вероватно последица непотпуности (мање) зависност афинитета комплекса лек-рецептор према трансдуктору. На пример, Делимични агонист опијатног рецептора налорфин делује слично пуном агонисту ових рецептора морфијуму., иако слабији од последњег. Истовремено, када се користе заједно, налорфин слаби или елиминише ефекте морфијума.; посебно, елиминише се инхибиторни ефекат морфијума на дисање. Изопреналин је прави агонист, а преналтерол је делимични агонист β-адренергичких рецептора. Према теорији рецептора, прави агонист може изазвати максималан одговор, чак и ако ступа у интеракцију само са делом рецептора.
Специфични рецептори могу имати иста или различита места везивања за агонисте и антагонисте.. Могућа различита места везивања за различите агонисте. У предмету, када агонист и антагонист имају иста места везивања и блокирајући ефекат антагониста на рецептор је потпуно елиминисан повећањем концентрације агониста (постиже се максимални ефекат агониста), однос између антагониста и агониста се означава као конкурентски антагонизам. Ако су места везивања за агонист и антагонист различита, онда се однос међу њима дефинише као нетакмичарски антагонизам. ПА индекс се често користи за карактеризацију антагониста.2 (негативни логаритам моларне концентрације антагониста, да би се постигао стандардни ефекат агониста, његова концентрација се мора удвостручити).
У условима целог организма, агонисти и антагонисти изазивају промене у одређеним физиолошким функцијама.. Дејство антагониста у овом случају је одређено, да ометају специфичне рецепторе одговарајућих природних лиганада (на пример, Антагонист М-холинорецептора атропин омета дејство њиховог агониста ацетилхолина). Промене, који су директно повезани са интеракцијом супстанци са специфичним рецепторима, који се назива примарни фармаколошки одговор, што може бити почетак читавог низа реакција, што доводи до стимулације или инхибиције одређених физиолошких функција".
Промене у функцијама органа или система (на пример, промене у јачини и учесталости срчаних контракција, тонус глатких мишића унутрашњих органа, секреције жлезда, АД итд.), изазвана лековима, означен као фармаколошки ефекти супстанце. Од, за срчане гликозиде, примарна фармаколошка реакција је инхибиција активности транспорта На +, К-АТП-азе влакана миокарда, који се сматра могућим специфичним рецептором за срчане гликозиде. С тим у вези, поремећен је проток К + у мишићна влакна и ослобађање На + из влакана., повећава се садржај Ца2+ у цитоплазми, што подстиче интеракцију актина и миозина. Резултат ових промена је повећање снаге срчаних контракција., који је главни фармаколошки ефекат срчаних гликозида.
Продужено излагање агониста специфичним рецепторима често је праћено смањењем њихове осетљивости.. Ово последње може бити повезано са променом рецептора, смањење њиховог броја (густина) или поремећај процеса, који прате ексцитацију рецептора. Истовремено, фармаколошки ефекти агониста постају мање изражени..
Тако, фармаколошки ефекти већине лекова повезани су са њиховим деловањем на одговарајуће специфичне рецепторе.
Супстанце са високим афинитетом за биорецептор и ниском интринзичном активношћу називају се антагонисти., или блокатори, јер они, без изазивања промена у конформацији биорецептора, спречавају интеракцију ендогених и/или егзогених агонистичких лиганда са њим. Постоје и такозвани „секундарни или тихи рецептори, са којима се вежу лекови, али нема фармаколошке активности. Такви "тихи" рецептори најчешће су присутни у протеинима и крвној плазми. (али се могу наћи и у ткивима). Веза са "тихим" рецепторима доводи до смањења концентрације слободног лека, а самим тим и смањити терапијски ефекат..
Бројне модерне теорије, објашњавајући механизам интеракције лиганд-рецептор, стање самих рецептора, недостатак пропорционалности између броја заузетих рецептора и коначног одговора, промена ефикасности преноса сигнала и постојање резервних рецептора и парцијалних агониста итд.. д. формирао је основу идеја о механизму деловања представника различитих група лековитих супстанци. Ове интеракције се деле на интеракцију са рецепторима и хемијску интеракцију..
Механизам интеракције лекова са биорецептором може се представити као следећи дијаграм: сваки лиганд (лековита супстанца или физиолошки супстрат) везује се за одређено место на одређеном рецептору. Активирани рецептори директно или индиректно регулишу ток јона (1) и/или други интрацелуларни процеси (секреција или контракција мишића) или активира протеински систем који везује нуклеотиде гванина (Г протеини), да, заузврат, појачава активацију другог интермедијарног ензимског система. У цитоплазми функционише неколико различитих секундарних гласника, активирање различитих циљних протеина, нпр. протеина- киназе. Потоњи делују на специфичне супстрате и посредују у фармаколошком ефекту.
Из датог описа, изгледа, да се деловање лекова спроводи следећим механизмима:
- физиолошке функције ткива (на пример, контрактилне, секреторни) могу регулисати више рецептора, и стога, и разни лиганди;
- може постојати неколико средњих корака између интеракције лека са рецептором и одговора ткива или органа, посебно, активација система секундарних гласника повезаних са рецепторима;
- ефикасност механизама, одговоран за секвенцу стимуланс-одговор, као и густина рецептора може да варира од ткива до ткива.
Терапеутски ефекат неких лекова је због њиховог директног (нису повезани са специфичним рецепторима) хемијска интеракција са ендогеним једињењима или други механизми интеракције (осмотски притисак, адсорпција). Дакле, за осмотске диуретике - манитол, уреа - нема специфичних рецептора. Ове супстанце повећавају осмотски притисак у бубрежним тубулима., што доводи до поремећене реапсорпције воде и повећане диурезе. Акција адсорбујућих супстанци није повезана са специфичним рецепторима., диуретици који формирају киселину.
Антациди (на пример, хидроксиди алуминијума или магнезијума) реагују са хлороводоничном киселином и формирају производе са благо киселим својствима. Средства за хелирање, везивање са одређеним металима, формирају неактивне хемијске комплексе.
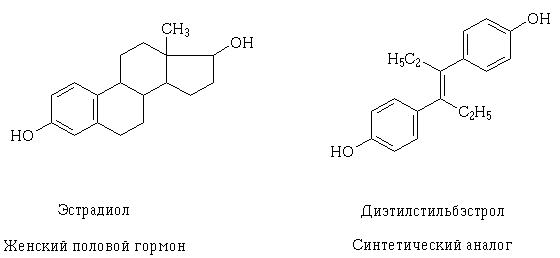
Како су се продубљивала сазнања о структури рецептора и механизму могуће фармакодинамичке интеракције лекова на ћелијском нивоу, постало је могуће њихово наменско креирање., као и објашњење, зашто лекови могу имати такав ефекат, различит, на први поглед, његову структуру. Пример таквог феномена је естрадиол и трансизомер диетилстилбестрола, синтетичког аналога женског полног. Њихови структурни молекули су различити, али садрже иста својства и величине функционалних хидроксилних група, слично лоцирани и оријентисани у простору, због чега молекули ових супстанци могу да комуницирају са истим рецептором и имају сличан фармаколошки ефекат.
Начини, које лековите супстанце изазивају одређена фармаколошка дејства, који се називају "механизми деловања". Овај концепт се користи да објасни деловање лекова на молекулу, нивоа органа и система. На пример, механизам деловања антихолинестеразе на молекуларном нивоу своди се на блокаду ацетилхолинестеразе интеракцијом са њеним ањонским и естеразним центрима. Међутим,, објашњавајући механизам антихипертензивног дејства антихолинестеразе, указују на брадикардију и вазодилатацију као узрок овог ефекта, Т. то је. размотрити механизам овог ефекта на нивоу органа.
Истраживања механизама деловања лекова су у току., штавише, идеје о механизму деловања одређене лековите супстанце, како се добијају нови подаци, не могу само да постану детаљније, али и значајно променити..
