Vasculare-plachetare hemostaza – Sistemul de hemostaza
Endoteliul, Camera suprafeței interioare a vaselor sanguine, Ea are o mare tromborezistentnost'ju şi joacă un rol important in mentinerea lichidului circulant sânge. Această proprietate a endoteliului asociate cu următoarele caracteristici:
- capacitatea de a forma şi de a oferi un inhibitor de agregarea trombocitelor sângelui puternic — prostaciclinei (metabolitul acidului arahidonic, referindu-se la prostaglandine);
- producţia de ţesături Activator fibrinolizei;
- incapacitatea de a contacta activarea sistemului de coagulare a sângelui;
- unitate de capacitate antikoaguljantnogo la graniţa de sânge/ţesut prin endoteliul comite Complexul heparină-antitrombină III;
- posibilitatea de a şterge din sange activat factorilor de coagulare.
Cu toate acestea, peretele vaselor de sânge, datorită caracteristicilor sale anatomice şi fiziologice-rigiditate, elasticitatea, plasticitate şi alţii — poate rezista nu numai tensiunii arteriale, dar moderat efecte traumatice externe, astfel încât acestea împiedică hemoragiile. Această proprietate, ca abilitatea de a rezista la intrarea de celule roşii din sânge de capilare de diapedeza, t. este. prin peretele vascular mecanic intacte, depinde pe utilitatea endoteliul şi caracteristicile structurii subjendotelial'nogo strat este gradul de dezvoltare şi calitatea de colagen si microfibra, corelatia dintre colagen si fibre elastice, structura membranei bazale şi t. d. Aceste proprietăţi sunt extrem de dependentă de cantitatea şi caracteristicile calitative ale trombocitelor, в силу чего при недостаточном их содержании в крови и (sau) при тромбоцитопатиях усиливаются как диапедезная кровоточивость, так и ломкость микрососудов: легко возникают петехии и кровоподтеки, devin pozitive probe pentru fragilitatea capilară -pinch, manzhetochnaja, borcan pe şi. ȘI. Nesterov şi altele.
Mikrososudy отвечают на повреждение выраженным локальным спазмом — рефлекторным и связанным с освобождением из стенок сосудов и тромбоцитов адреналина, noradrenalinei, serotonina si alte substante biologic active.
Daune la pereţii vaselor de și, în special, оголение субэндотелия способствуют активации свертывания крови и тромбоцитарного гемостаза несколькими путями:
- выделением в кровь тканевого тромбопластина (factorul III, apoproteină C) и других активаторов свертывания и агрегации тромбоцитов — адреналина, noradrenalinei, АДФ и др.;
- контактной активацией коллагеном и другими компонентами субэндотелия как тромбоцитов (адгезия), так и свертывания крови (активация фактора XII);
- продукцией плазменных кофакторов адгезии и агрегации тромбоцитов — фактора Виллебранда и др.
Astfel, стенка сосудов тесно связана и взаимодействует со всеми другими звеньями системы гемостаза, особенно с тромбоцитами.
Участие тромбоцитов в гемостазе определяется в основном следующими их функциями:
- ангиотрофической — способностью поддерживать нормальную структуру и функцию микрососудов, их устойчивость к повреждающим воздействиям, непроницаемость по отношению к эритроцитам;
- способностью поддерживать спазм поврежденных сосудов путем секреции (реакции освобождения) вазоактивных веществ — адреналина, noradrenalinei, серотонина и др.;
- способностью закупоривать поврежденные сосуды путем образования первичной тромбоцитарной пробки (тромба), включающей приклеивание тромбоцитов к субэндотелию (адгезивная функция), склеивание их друг с другом и образование комков из набухших тромбоцитов (агрегационная функция), а также синтез, накопление и секрецию при активации веществ, стимулирующих адгезию и агрегацию;
- тромбопластической — способностью тромбоцитов выделять гемостатические факторы.
Все приведенные данные позволили обосновать учение о единстве сосудисто-тромбоцитарного, или первичного, гемостаза. Основанием для этого учения послужило классическое исследование Дьюка, показавшее, că timpul de sângerare în piele de lobul urechii puncție acul sau acul (proba Dyyuka) crește în mod regulat cu trombocitopenie severă, dar rămâne normală sau aproape normală în tulburări hemoragice adânci (de exemplu,, Hemofilie). Aceste date, Obțineți confirmarea deplină în studii suplimentare, condus la concluzia, că hemostaza primara in microvessels se datorează în principal de trombocite. Această creștere semnificativă a timpului de sângerare este înregistrat nu numai cu trombocitopenie semnificative (T în mai puțin de 30-50 1 L), dar în formele severe de inferioritate calitativă de trombocite (Glanzmann Trombastenia, trombocytopathies), precum disfuncție a celulelor de origine secundar - din cauza lipsei de plasmă cofactori adeziunea și agregarea în plasmă sau prezența inhibitorii acestor funcții (paraprotein, Produsele proteoliza și altele.).
Среди наследственных форм вторичной дисфункции тромбоцитов наиболее важной и распространенной в клинической практике является angiogemofiliya (boala von Willebrand), при которой время кровотечения увеличивается до 0,5—1 ч и более, а из приобретенных форм — нарушения функции тромбоцитов при диссеминированном внутрисосудистом свертывании крови (тромбоцитопатия потребления, повреждающее действие продуктов протеолиза), uremie, consumul de droguri (aspirină, antykoahulyantы, фибринолитики и др.).
Формирование тромбоцитарной пробки и остановка кровотечения из микрососудов завершается при проведении пробы Дьюка за 2—4 мин, а при создании дополнительного венозного стаза (наложение манжеты с давлением 5,3 kPa, sau 40 mm Hg. Art., Și altele) — за 6—10 мин.
Ведущая роль в реализации первичного гемостаза принадлежит адгезивно-агрегационной функции тромбоцитов (AAFT).
В настоящее время достаточно хорошо изучены основные механизмы ААФТ, разработаны доступные лабораторно-инструментальные методики ее исследования. Чаще всего пусковую роль в этом процессе играет повреждение стенки кровеносных сосудов, вследствие чего тромбоциты вступают в контакт с субэндотелием, в частности — с главным стимулятором адгезии коллагеном, umfla, образуют отростки и приклеиваются (адгезируют) на этих участках.

Важнейшими плазменными кофакторами этого процесса являются ионы кальция и синтезируемый в эндотелии белок—Factorul von Willebrand (factor VIII: RKOF) а в тромбоцитах — взаимодействующий с фактором Виллебранда мембранный гликопротеин Euîn (ГП-Euîn).
В связи с этим дефицит фактора Виллебранда (angiogemofiliya, sau boala von Willebrand) или ГП-Iв (trombotsitodistrofiya, или болезнь Бернара—Сулье) сопровождается резким нарушением адгезивности тромбоцитов.
Наряду с адгезией протекает процесс агрегации тромбоцитов — набухания и склеивания их между собой с образованием отростков и с наложением агрегатов на участок повреждения сосуда, в силу чего гемостатическая пробка или тромб быстро растет.
Первичный стимул к агрегации дают коллаген, выделяющийся из поврежденных стенок сосудов, и в еще большей степени АДф из гемолизирующихся в зоне повреждения эритроцитов, катехоламины и серотонин (L. 3. Баркаган, B. F. Архипов, 1980, 1983).
Из тромбоцитов, подвергающихся адгезии и агрегации, активно секретируются гранулы, которые содержат вещества, усиливающие процесс агрегации и формирующие ее вторую волну. Acestea includ небелковые гранулы высокой электронно-оптической плотности, содержащие в большом количестве АДФ, adrenalina, норадреналин и серотонин, а также α-гранулы, содержащие белки — антигепариновый фактор (factor 4), β-тромбоглобулин, тромбоцитарный стимулятор роста (митогенный фактор) și etc.
Позднее секретируются гранулы, содержащие лизосомальные ферменты (реакция освобождения II).
В результате взаимодействия тромбоцитарных и плазменных факторов в зоне гемостаза образуется тромбин, малые дозы которого резко усиливают и завершают процесс агрегации и одновременно вызывают свертывание крови, в силу чего тромбоцитарный сгусток покрывается фибрином, приобретает большую плотность, подвергается ретракции.
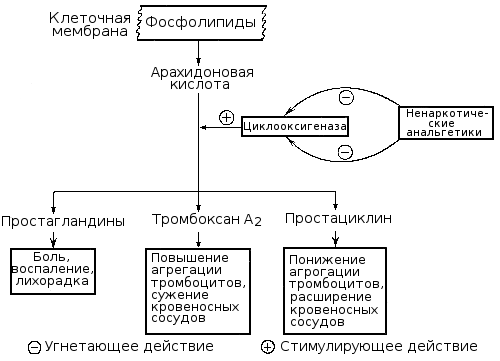
Чрезвычайно важную роль в регуляции тромбоцитарного гемостаза играют производные арахидоновой кислоты, освобождаемой из мембранных фосфолипидов тромбоцитов и стенки сосудов вследствие активации фосфолипаз.
В дальнейшем под влиянием циклооксигеназы из арахидоновой кислоты образуются prostaglandine (PGG2, PGH2), а из них в тромбоцитах под влиянием тромбоксансинтетазы вырабатывается чрезвычайно мощный агрегирующий агент — тромбоксан A2 (TXA2), а в стенке сосудов под влиянием простациклинсинтетазы — основной ингибитор агрегации — простациклин (простагландин Eu2, PGI2).
Нарушение образования тромбоксана A2 в результате снижения активности или блокады циклооксигеназы или тромбоксансинтетазы ведет к выраженному нарушению функции тромбоцитов, способствует развитию кровоточивости, что наблюдается при ряде наследственных и приобретенных (симптоматических) тромбоцитопатий. Нарушение же синтеза в стенке сосудов простациклина или ослабление его поступления в кровь ведет к повышенной склонности тромбоцитов к агрегации, создает тромбогенную опасность. Продолжительность активного действия тромбоксана, простациклина и родственных им других простагландинов небольшая (Un câteva minute), но значение их в регуляции и патологии гемостаза весьма велико. В результате метаболизма они превращаются в неактивные производные — тромбоксан B2 и другие конечные продукты.
Potrivit oamenilor de știință, исследование которых легло в основу учения о простагландиновой регуляции тромбоцитарного гемостаза, этот механизм является пусковым в развитии адгезивно-агрегационной функции тромбоцитов. Активация тромбоцитарных мембран может осуществляться не только АДФ и тромбоксаном, но и гидроперекисями полиненасыщенных жирных кислот, образующимися в ходе свободнорадикального аутоокисления фосфолипидов.
Помимо перечисленных выше агентов, в тромбоцитах и в других активированных клетках крови (лейкоцитах и пр.) образуются и иные мощные стимуляторы агрегации. Из них в последние годы особое внимание уделяется фосфолипидному пластиночному агрегирующему фактору (PAF) из лейкоцитов и тромбоцитов, являющемуся 1-0-октадецил-2-ацетил-3-фосфорилхолином, а также содержащемуся в α- гранулах тромбоцитов гликопротеину G (тромбоспондин, эндогенный лектин). Этот фактор освобождается из тромбоцитов вместе с α-гранулами, фиксируется на поверхности активированных кровяных пластинок, образуя комплекс с фибриногеном, и в таком виде используется для осуществления тромбинагрегации. В силу этого при тромбоцитопатиях с отсутствием α-гранул (de exemplu,, при синдроме серых тромбоцитов) нарушается агрегация этих клеток под влиянием тромбина.
Для осуществления адгезивно-агрегационной функции тромбоцитов необходим ряд плазменных кофакторов агрегации — ионы кальция и магния, fibrinogen, альбумин и два белковых кофактора, именуемые агрексонами A и B, фосфолипидный кофактор и др.
Вместе с тем парапротеины, криоглобулины и продукты фибринолнза ингибируют агрегацию тромбоцитов. К белковым ингибиторам этого процесса относятся также простациклин – зависимый макромолекулярный белок, фактор Барнес—Лиана (резко снижается при тромботической тромбоцитопенической пурпуре) și etc.
В осуществлении агрегационной функции важную роль играют мембранные гликопротеины тромбоцитов, взаимодействующие с агрегирующими агентами.
Согласно рекомендациям Международного комитета по тромбозам и гемостазу, различают следующие основные виды мембранных гликопротеинов:
Гликопротеин I, состоящий из двух субъединиц — Ia и Ib. Первая из них является рецептором фактора Виллебранда и необходима для адгезии, а вторая — для тромбин-агрегации. Содержание гликопротеина I снижено при одной из вариантных форм ангиогемофилии и при тромбоцитодистрофия (Boala Bernard-Soulier).
Гликопротеин II, также состоящий из двух субъединиц, необходим для всех видов агрегации, содержание его (особенно IIb) резко снижено при тромбоцитоастении Гланцманна.
Гликопротеин III, одни из компонентов которого соединяется с гликопротеином IIb и кальцием, необходим для большинства видов агрегации и ретракции сгустков; содержание его снижено при тромбоцитоастении Гланцманна
Функциональное значение IV и V мембранных гликопротеинов нуждается в уточнении.