Kajian pembekuan darah
Kaedah penyiasatan sistem pembekuan darah termasuk kumpulan-kumpulan berikut:
- indikatif (bersama-sama), memberi idea mengenai keadaan keseluruhan pembekuan lata secara keseluruhan dan peringkat individu (pendaftaran boleh dibuat secara visual atau dengan peranti individu - koagulografa, Thromboelastography et al.);
- membezakan defisit faktor individu - ujian pembetulan pembekuan, Ujian mencampurkan darah dengan kajian plasma darah plasma dalam pesakit yang kekurangan dikenali diketahui faktor-faktor tertentu;
- quantitation komponen individu kepada aktiviti kerja mereka seperti sistem (ujian pembekuan, kajian dan substrat chromogenic lain) dan (atau) pada penanda imunologi;
- выявления внутрисосудистой активации процесса свертывания крови и фибринолиза по функциональным признакам или молекулярным маркерам такой активации — выявлению в циркуляции активированных факторов свертывания, продуктов дегрануляции тромбоцитов, расщепления компонентов свертывающей системы крови или их метаболитов, появлению новых антигенных маркеров активированных факторов и их комплексов, dipercepatkan komponen metabolisma dilabel sistem pembekuan darah (mengurangkan tempoh separuh hayat mereka dalam edaran).
Oleh itu, dalam penilaian pembekuan darah digunakan dengan betul prosedur pembekuan (makmal dan instrumental), menjadi asas proses diagnostik, dan imunologi, radionuklid dan bentuk-bentuk kajian. Dalam banyak kes, komponen sistem boleh ditakrifkan sebagai aktiviti berfungsi, dan immunologikal - kandungan antigen yang berkenaan dalam darah. digunakan serentak teknik seperti membolehkan untuk membezakan bentuk patologi, связанные с отсутствием синтеза соответствующего фактора свертывания (в этом случае одинаково снижены как его функциональная активность, так и количество антигена), и формы, при которых молекула фактора синтезируется, но она аномальна и функционально неполноценна.
Для обозначения первых форм к номеру соответствующего фактора добавляется знак «—» (sebagai contoh, VIII-, (IX)- dll. d.), dan di kedua - tanda "+" (sebagai contoh, VIII +, IX +).
anggaran (bersama-sama) pembekuan ujian
Penentuan masa pembekuan darah
Penentuan masa pembekuan darah (kaedah pilihan Lee-White) - telah lama digunakan bystrovypolnimy (di sisi katil itu) ujian menunjukkan, yang membolehkan untuk mengenal pasti gangguan pendarahan yang ketara, yang dikaitkan dengan kekurangan faktor pembekuan darah (kecuali Factor VII) atau tindakan anticoagulants dan fibrinolytics. Ia digunakan sebagai panduan untuk ujian dan kawalan terapi heparin, penghapusan heparin protamine sulfat. Тест сравнительно низкочувствительный, показатели его нарушаются лишь при выраженном снижении содержания в плазме факторов свертывания (ниже 4—5 %), berkaitan dengan apa yang tidak sesuai untuk mengesan hemofilia ringan A dan B, serta gangguan pembekuan di angiohemophilia, kekurangan Factor XI, prekallikrein, dan berat badan tinggi kininogen molekul. Untuk sebab-sebab ini, ujian itu tidak boleh digunakan untuk penilaian pra operasi pesakit: di bawah prestasi ujian normal (5-10 min) возможно возникновение профузных послеоперационных кровотечений.
Время рекальцификации плазмы
Время рекальцификации плазмы — нестандартизированный низкочувствительный тест, kurang dipercayai untuk mengesan pencegahan penggumpalan darah, daripada seluruh masa pembekuan darah. Ia tidak boleh disyorkan untuk diagnosis gangguan hemostasis.
Активированное парциальное тромбопластиновое время плазмы
Активированное парциальное тромбопластиновое время плазмы (АПТВ, каолин-кефалиновый тест) — высокочувствительный метод, mengesan pelanggaran pembekuan apabila memulakan mekanisme dalaman proses. Terpilih sensitif kepada kekurangan faktor pembekuan plasma (sebagai kekurangan platelet dan faktor 3 Platelet pampasan cephalins luaran diinput atau eritrofosfatidom).
Ia digunakan untuk memantau heparin, pesakit pra operasi, dan lain-lain. d. petunjuk Standard bergantung kepada sampel kephaline digunakan, dalam kebanyakan kes sehingga 37-50 (secara optimum - 37-45 dengan).
Каолиновое время плазмы
Каолиновое время плазмы — тест, сходный с предыдущим, но без добавления в плазму кефалина (эритрофосфатида), в результате чего он чувствителен не только к дефициту плазменных факторов свертывания, но и к недостатку тромбоцитов и фактора 3 Platelet. Ориентировочная оценка активности этого фактора может быть проведена путем сравнения каолинового времени плазмы исследуемого с высоким и низким содержанием тромбоцитов (норма — 57—70 с).
Не рекомендуется использование фосфолипидных компонентов, дающих в АПТВ время свертывания равное 55 с и более, так как при этом резко снижается точность и воспроизводимость тестов, в том числе при количественном определении факторов VIII и IX.
Силиконовое время плазмы
Силиконовое время плазмы — это время рекальцификации плазмы, полученной в условиях силиконирования игл, пробирок, пипеток, t. ia adalah. при минимальной контактной активации. Тест чувствителен к гиперкоагуляции—внутрисосудистой активации пусковой контактной фазы (факторов XII и XI), однако это нарушение более четко выявляется путем определения силиконового времени свертывания цельной крови (на основе метода Ли—Уайта либо тромбоэластографической регистрации процесса в силиконированной кювете).
petunjuk Standard bergantung kepada silikon dan ditentukan dengan memeriksa darah orang yang sihat untuk setiap sampel secara berasingan. Apabila memilih silikon adalah yang terbaik, который в наибольшей степени удлиняет время свертывания крови (plasma).
Протромбиновое (тромбопластиновое) время плазмы
Протромбиновое (тромбопластиновое) время плазмы (время Квика, Indeks prothrombin) Ia menyifatkan kadar plasma recalcified pembekuan apabila memulakan mekanisme luaran proses, t. ia adalah. menambah otak manusia tromboplastin (atau arnab).
Активность тромбопластина стандартизируется на смешанных образцах нормальной (контрольной) plasma. Чаще всего используются тромбопластины активностью 12—18 с (в классической методике Квика— 12—13 с). The tromboplastin lemah, kaedah kesilapan yang lebih.
Dalam prothrombin normal ujian masa plasma mendedahkan kekurangan terpencil atau gabungan faktor-faktor kompleks prothrombin itu - VII, X, V dan II, di mana tiga faktor ((VII), X и II) K-vitaminozavisimy dan aktiviti mereka berkurangan di bawah pengaruh anticoagulants tidak langsung. Dalam hal ini, ujian prothrombin adalah asas dalam mengawal coumarins dos (neodikumarin, atau pelentan, sinkumar et al.) dan ubat-ubatan lain dalam kumpulan ini (fenilin).
Протромбиновое время остается нормальным при дефиците факторов внутреннего механизма активации протромбиназы — факторов XII, XI, (IX), VIII (t. ia adalah. при всех видах гемофилии и дефекте Хагемана), serta kekurangan prekallikrein dan berat tinggi kininogen molekul (VM kininogen)
Dalam kesusasteraan yang berbeza penetapan keputusan ujian prothrombin. Yang paling bermanfaat untuk menentukan ujian masa prothrombin dan mengawal plasma darah dalam saat (yang memberikan maklumat mengenai aktiviti dan tromboplastin yang digunakan). Kadang-kadang nisbah penggunaan kedua-dua nilai, t. ia adalah. indeks (PV kajian plasma, dengan ,)/(PT plasma kawalan, dengan), (kadar 0,9-1,1).
Satu lagi bentuk penilaian penunjuk ini, которой наиболее широко пользуются в лабораториях, является вычисление протромбинового индекса в процентах путем составления обратной арифметической пропорции (норма — 90—110%), Walau bagaimanapun, pengiraan ini adalah salah, kerana tidak ada aritmetik antara kepekatan faktor pembekuan dan masa pembekuan, hubungan logaritma. Lebih-lebih lagi, протромбиновый тест чувствителен лишь к снижению факторов свертывания ниже 50 % их нормальной величины. Atas sebab ini, adalah suai manfaat untuk menggunakan takrif Peratus indeks prothrombin keluk pencairan (1:2, 1:4, 1:8 dll. d.) sampel campuran plasma normal. Такая кривая строится однократно для тромбопластинов разной исходной активности (daripada 12 kepada 18 dengan) и по ней определяется протромбиновый индекс у исследуемых больных. Преимущество такой методики состоит также в том, что результаты всех исследований, в том числе и выполняемых в динамике в разные дни, соотносятся не к случайным различным образцам нормальной плазмы крови, а к усредненным одним и тем же стандартным параметрам, вследствие чего существенно уменьшается ошибка метода. indeks, diperolehi oleh bahagian dan pencairan lengkung plasma normal, tidak sesuai dengan satu sama lain. Это следует учитывать и при контроле за действием непрямых антикоагулянтов, ибо снижение обычного индекса до 50 % примерно соответствует снижению индекса по кривой разведения до 25—30 %• В связи с этим в анализах всегда следует указывать, как рассчитывался протромбиновый индекс, apakah standard prestasi bagi suatu aktiviti tromboplastin diberikan.
Plasma masa thrombin
Plasma masa thrombin, t. ia adalah. время свертывания цитратной плазмы при добавлении к ней тромбина стандартной активности, является основным тестом для оценки конечного этапа свертывания крови. Kemasukan penunjuk ini adalah penting bagi tafsiran yang betul semua ujian pembekuan lain, ибо нарушение конечного этапа свертывания крови неизбежно должно привести к удлинению времени свертывания во всех перечисленных выше методиках.
В большинстве случаев при проведении тромбинового теста используется такая концентрация раствора тромбина, которая при смешивании с равным объемом плазмы крови дает свертывание за 12— 18 dengan, tetapi digunakan semasa pengiktirafan disfibrinogenemy kepekatan lemah (yang membawa kepada pengurangan 30-35 saat).
masa thrombin - penunjuk diagnostik penting, нарушение его наблюдается как при врожденных, так и при часто встречающихся приобретенных (menengah) гипопротромбинемиях, при большинстве дисфибриногенемий, а также под влиянием гепарина, продуктов фибринолиза (Pdf) и ряда других антитромбинов и ингибиторов самосборки мономеров фибрина. Oleh kerana itu, masa thrombin di tempat pertama dan banyak lagi diganggu oleh akut dan subakut DIC, yang memainkan peranan penting dalam diagnosis pesat patologi ini.
ujian Autokoagulâcionnyj
ujian Autokoagulâcionnyj (kebenaran) - yang sangat sensitif dua langkah, Ia menerangkan proses pembekuan darah pada permulaan mekanisme dalaman. Seperti aPTT, тест не чувствителен к дефициту фактора VII, но вместе с тем его показания не зависят от содержания фибриногена (фактора I) в исследуемой плазме крови, bagaimana ia berbeza daripada semua sampel lain yang menunjukkan pembekuan.
Kelebihan lain adalah bahawa ACP, bahawa darah dicairkan disiasat, благодаря чему существенно повышается чувствительность теста к дефициту факторов свертывания и, lebih-lebih lagi, выполнение АКТ не требует использования каолина и кефалина, поскольку стандартизация контактной и фосфолипидной активации в нем достигается гемолизатом собственных эритроцитов исследуемого.
Сущность АКТ состоит в том, что к 2 мл гипотонического раствора (0,222 %) хлорида кальция добавляется 0,1 мл крови исследуемого.
В этой гемолизат-кальциевой смеси происходит образование протромбиназы и тромбина, Aktiviti ini telah dipilih oleh berurutan menambah 0,2 ml campuran ini kepada 0,2 ml ujian plasma (melalui setiap 2 min semasa pertama 10 m, dan kemudian - setiap 10 minit untuk 1 tidak).
Plasma adalah sumber fibrinogen disiasat, apabila aktiviti diuji dalam campuran thrombin dibentuk. Seperti yang ditunjukkan oleh banyak kajian, она может быть заменена плазмой крови здоровых людей или раствором фибриногена. В этом случае расход крови больного сокращается до 0.1—0,2 мл (может быть взята из пальца!), yang трансформирует аутокоагуляционный тест в микрокоагуляционный (МКТ) и делает его очень удобным для использования в педиатрии, в том числе при исследовании гемостаза у новорожденных.
aktiviti pembekuan dalam ACP dan MKT mulanya meningkatkan pada orang yang sihat biasanya mencapai maksimum 10 minit,, Pengeraman campuran darah kalsium (KKS), когда свертывание субстратной плазмы происходит за 10±1 с. Затем коагуляционная активность ККС начинает снижаться, что свидетельствует об инактивации образовавшегося в ней тромбина. При гемофилиях, действии гепарина и других нарушениях свертываемости коагулирующая активность ККС резко снижается, а максимум перемещается с 10-й минуты на более поздний срок. При гиперкоагуляции наблюдается более раннее и более значительное нарастание тромбиновой активности в ККС.
При проведении теста в одной пробирке (definisi hanya pada KKS pengeraman minit ke-10) ia boleh digunakan untuk memantau terapi heparin. Преимущество этой методики перед тестом активированного парциального тромбопластинового времени состоит в том, что в ней нивелируется неодинаковое влияние разных кефалинов на гепариновое время свертывания.
На основе АКТ (МКТ) разработана простая и точная методика дифференциальной диагностики гемофилий.
С помощью приводимых в справочниках переводных таблиц показания АКТ (МКТ) boleh dinyatakan sebagai peratusan dan graf - autokoagulogrammy.
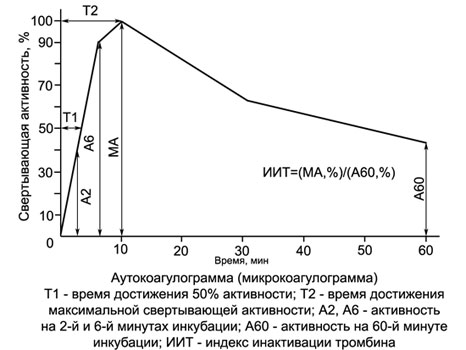
Для оценки ряда общих параметров свертываемости крови широко используются и инструментальные методы исследования, advantageously menggunakan koagulografov berbeza dan thromboelastography.
thromboelastography Ia memberi idea bukan sahaja parameter masa darah atau plasma pembekuan, tetapi juga pada struktur dan mekanikal sifat beku terbentuk. В последние годы и в аппаратные методы регистрации вводится стандартизация контактной и фосфолипидной активации процесса свертывания. Создаются также коагулограммы для массового выполнения общих коагуляционных тестов — АПТВ, протромбинового, тромбинового и других с автоматической записью результатов.
Методы дифференциации дефицита различных факторов свертывания и их количественного определения
Приведенные ниже в таблице данные показывают, что ориентировочное исследование свертываемости крови с помощью трех основных тестов позволяет провести групповое разграничение дефицита различных плазменных факторов гемокоагуляции. Sejak, замедление свертываемости только в протромбиновом тесте (I тип нарушения) при нормальных показаниях всех остальных характерно для наследственного дефицита фактора VII либо для снижения уровня этого фактора на ранних этапах развития механической желтухи или в первые 1—2 дня лечения антикоагулянтами непрямого действия, когда подавление синтеза фактора VII опережает в своем развитии снижение уровня всех остальных К-витаминозависимых факторов свертывания.
Типы нарушений основных коагуляционных тестов при дефиците тех или иных плазменных факторов свертывания | ||||
Тип нарушений | Дефицитные факторы в исследуемой плазме крови | Коагуляционные тесты | ||
АПТВ, kebenaran | ПВ | ТВ | ||
| Saya | (VII) | – | + | – |
| II | XII | + | – | – |
| XI | + | – | – | |
| (IX) | + | – | – | |
| VIII | + | – | – | |
| Фактор Виллебранда | + | – | – | |
| Плазменный прекалликреин | + | – | – | |
| ВМ кининоген | + | – | – | |
| Iii | II | + | + | – |
| Dalam | + | + | – | |
| X | + | + | – | |
| (VII) | – | + | – | |
| (IX) | + | – | – | |
| Saya | + | + | + | |
| XIII | – | – | – | |
| (IV) | Антикоагулянты прямого действия (Heparin, гепариноиды и др.) | + | + | + |
| Антикоагулянты непрямого действия (coumarins) | + | + | – | |
| Nota kaki. (+) — замедление свертывания; (-) — отсутствие нарушения свертывания. | ||||
Нарушение только внутреннего механизма свертывания, t. ia adalah. активированного парциального тромбопластинового времени и АКТ (II тип), наблюдается при дефиците факторов XII, XI, (IX), VIII, Виллебранда (не при всех формах), прекалликреина и ВМ кининогена. Из них при наследственных дефектах свертываемости дефицит факторов XII, прекалликреина и ВМ кининогена наблюдается крайне редко и не сопровождается какой-либо кровоточивостью, тогда как дефицит факторов VIII (гемофилия А), (IX) (гемофилия В) и фактора Виллебранда встречается очень часто (составляет более 96 % всех наследственных коагулопатий) и сопровождается выраженной кровоточивостью. Между ними в первую очередь и проводится дальнейшая дифференциальная диагностика.
Дефицит фактора XI встречается сравнительно редко (около 0,5—1,0 % всех гемофилий), протекает с очень слабо выраженной кровоточивостью (в основном после травм и операций) и занимает промежуточное место между первой подгруппой бессимптомных нарушений и гемофилиями и болезнью Виллебранда.
Еще один тип нарушений характеризуется удлинением как парциального тромбопластинового времени и АКТ, так и протромбинового времени. Он характерен для дефицита факторов V, X atau II atau yang kekurangan kompleks faktor-K vitaminozavisimyh ((VII), X, (IX), II), yang diperhatikan dalam jaundis obstruktif dan lain-lain bentuk kekurangan K-vitamin, а также при приеме антикоагулянтов непрямого действия.
Dan akhirnya, как видно из той же таблицы, возможно нарушение показаний всех трех тестов (IV тип), что наблюдается при наследственных и приобретенных гипо- и дисфибриногенемиях (не всех), при приеме антикоагулянтов прямого действия (heparin, гепариноидов, гирудина и др.), лечении активаторами фибринолиза и дефибринирующими препаратами (стрептокиназа, урокиназа и др.), появлении в крови патологических антитромбинов и веществ, препятствующих соединению (сборке) фибрин-мономеров — парапротеинов, криоглобулинов, иммунных комплексов, а также при сложных нарушениях свертываемости, обусловленных ДВС-синдромом. При этом тромбиновое время часто нарушается в большей степени и несколько раньше, чем другие тесты.
При учете давности заболевания и возможности его наследственного генеза либо вторичной связи с другими видами патологии и лекарственными или иными воздействиями, наличия или отсутствия кровоточивости и ее типа удается правильно определить генез этих глубоких нарушений свертывания крови.
Semua дифференцирующие тесты основаны на принципе коррекции, t. ia adalah. на определении, в какой степени выявленное нарушение свертываемости крови устраняется или, sebaliknya, не устраняется образцами плазмы крови или искусственно полученными препаратами крови с заведомо известным дефицитом того или иного фактора свертывания.
С этой целью специализированные лаборатории создают для себя коллекции фактородефицитных плазм крови, получая их от больных с заведомо установленным глубоким (kurang 1 %) kekurangan setiap faktor, dan menyimpannya di dalam pakej kecil (pada 0,5 ml) pada suhu - 30 ° C. Jika perlu, sampel ini dicairkan dan digunakan dalam ujian diagnostik.
Plasma, telah sengaja atau unfreeze yang tidak digunakan selebihnya, pembekuan semula tidak tertakluk kepada. В коррекционных тестах не следует использовать плазму с иммунными ингибиторами того или иного фактора. В диагностических наборах ряда фирм содержатся лиофильно высушенные образцы плазмы крови с дефицитом определяемых факторов свертывания (субстратные плазмы). Walau bagaimanapun, banyak gangguan pendarahan jarang dilihat dalam amalan klinikal, в связи с этим используются искусственно приготовленные компоненты нормальной крови с дефицитом тех или иных факторов свертывания, а также гетерогенные плазмы (цыплят, утят и др.).
В таблице приведены сведения о содержании факторов свертывания крови в компонентах крови, digunakan untuk pembetulan ujian pembekuan, bergantung kepada syarat-syarat penyimpanan mereka. Menggunakan jadual ini, mudah untuk mentafsirkan bacaan mana-mana tiga ujian pembekuan utama. Teknik pembetulan seumpamanya menggunakan ini ujian, стандартизированные по контакту и фосфолипидной активации, t. ia adalah. каолин-кефалиновые или с применением гемолизата (в АКТ).
Содержание факторов свертывания а плазме крови с различными сроками хранения, используемой для проведения коррекционных тестов | ||
Плазма крови | Фактор свертывания | |
внутреннего механизма | mekanisme luaran | |
VIII IX XI XII prekallikrein | VII X V II | |
| native speakers (dengan jangka hayat sehingga 18 tidak) | ++++ | ++++ |
| terjerap * | +-++ | –+- |
| Dengan jangka hayat lebih daripada 24 tidak | -+++ | ++– |
| Dengan jangka hayat 2-4 hari (di + 4 ° C) | tidak digunakan | ++-+ |
| Профильтрованная ** | tidak digunakan | –++ |
| Нативная плазма цыплят или утят (в возрасте до 3—4 дней) | +++- | tidak digunakan |
| Nota kaki. (+) — наличие фактора; (-) — отсутствие. | ||
| * Адсорбция производится либо сульфатом бария из оксадаткой плазмы (BaSO4-plasma). либо гелем гидроокиси аллюминня из цитратной плазмы (Al(OH)3-plasma). | ||
| ** Фильтрация производится через два асбестовых фильтра (фильтры Зейца) — с 20 % (верхний фильтр) dan 30 % (нижний фильтр) kandungan asbestos atau melalui dua kali ganda atau tiga kali ganda, masing-masing 30 dan 20 % penapis. | ||
ujian plasma bergaul dengan plasma darah pesakit, имеющей заведомо известный дефицит того или иного фактора
Определяют активированное парциальное тромбопластиновое время в исследуемой плазме крови, нормальной плазме (контроль) и в плазме с заведомо известным дефицитом факторов VIII (от больного гемофилией А), (IX) (от больного гемофилией В), XI и XII. Затем готовят смесь из образцов цитратной плазмы исследуемого (7/10 объема) и последовательно с каждой из дефицитных плазм (3/10 объема), начиная с дефицита фактора VIII и IX (наиболее частые формы патологии!).
К смеси добавляют каолин и кефалин, dan oleh 2 мин подвергают ее рекальцификации (при температуре 37 ° C). В той смеси, где активированное парциальное тромбопластиновое время не нормализуется, имеется один и тот же дефект свертывания.
Sejak, если у обследуемого больного активированное парциальное тромбопластиновое время не нормализуется добавлением плазмы крови больного с заведомо известным дефицитом фактора VIII, но корригируется плазмой крови больного с дефицитом фактора IX, у него имеется гемофилия А.
Begitu juga,, но на основе протромбинового теста дифференцируют дефицит факторов протромбинового комплекса (X, Dalam, VII и II).
Тест генерации тромбопластина
Для дифференциации нарушений внутреннего механизма свертывания крови чаще всего используется классический тест генерации тромбопластина с заменой тромбоцитарного компонента, приготовление которого требует значительной затраты времени и крови, кефалином Недостатками теста генерации тромбопластина являются его громоздкость, необходимость приготовления большого числа реагентов, значительная затрата времени на его выполнение.
Коррекционный тест, основанный на базе аутокоагуляционного теста.
Задачам экспресс-диагностики вполне отвечает другой коррекционный тест, основанный на проведении коррекции теми же компонентами нормальной крови на базе аутокоагуляционного теста.
Этот тест отличается высокой надежностью, быстротой и легкостью выполнения и требует небольшого (max 0,5 ml) количества крови исследуемого, что позволяет использовать его в педиатрической практике.
В нем, как и в тесте генерации тромбопластина, используют для коррекции адсорбированную плазму и старую сыворотку крови, которую повторно центрифугируют перед проведением исследования. Tiga tiub dicurahkan 2 ml 0,222 % larutan kalsium klorida, dan dalam dua daripada mereka ditambah 0,1 ml terjerap plasma normal (1-Saya vial) dan 0,1 serum normal ml lama (2-Saya vial). В три другие пробирки вносят по 0,2 мл нормальной цитратной плазмы. Затем во все пробирки с раствором хлорида кальция добавляют по 0,1 мл цитратной крови исследуемого.
Ровно через 4 мин инкубации этой смеси ее свертывающую активность тестируют на нормальной плазме.
Резкое снижение коагулирующей активности только в первой пробирке (с нормальной BaSO4-плазмой) Ia menunjukkan kehadiran kekurangan IX faktor pesakit (гемофилия В), Hanya dalam tiub kedua (dengan serum lama) - defisit faktor VIII (гемофилия А); jika pembetulan berlaku dalam dua tabung uji (sama kuat), kemudian, jelas, terdapat kekurangan faktor XI atau XII (melihat. Jadual. 14).
Коагуляционные тесты, membezakan gangguan pembekuan darah mekanisme dalaman (di normal prothrombin dan thrombin masa) | |||
Дефицитные факторы в исследуемой плазме крови | komponen darah yang normal, ditambah kepada plasma disiasat | ||
plasma terjerap (ada faktor IX) | serum lama (ada faktor VIII) | Campuran telah terjerap plasma dan lama serum | |
| faktor VIII | + | – | + |
| faktor IX | – | + | + |
| Faktor XI atau XII | + | + | + |
| Nota kaki. (+) — нормализация свертывания; (-) — отсутствие нормализации свертывания. | |||
Данный тест высокочувствителен, так как исследование проводится на разведенной в 20 раз крови при компенсации фактора 3 тромбоцитов гемолизатом. Единственный используемый реактив — гипотонический раствор хлорида кальция, что делает пробу общедоступной.
Столь же простой является методика коррекционных проб, выполняемых на основе протромбинового теста для дифференциации дефицита факторов II, V и VII+, X (в таблице).
Коагуляционные тесты, дифференцирующие дефицит факторов II, V и VII+, +X, выполняемые на основе протромбинового теста (при нормальном тромбиновом времени) | ||||
Дефицитные факторы в исследуемой плазме крови | komponen darah yang normal, ditambah kepada plasma disiasat | |||
plasma terjerap (без факторов II, (VII), X) | Старая плазма (без фактора V) | Профильтрованная плазма (без факторов VII и X) | serum lama (без факторов II и V) | |
| Факторы VII или X | – | + | – | + |
| Фактор V | + | – | + | – |
| Фактор II | – | + | + | – |
| Nota kaki. (+) — нормализация свертывания; (-) — отсутствие нормализации свертывания. | ||||
Для того чтобы разграничить дефицит факторов VII и X, выполняется дополнительный коагуляционный тест с добавлением к исследуемой плазме крови раствора яда змеи гюрзы — препарат лебетокс (подбирается такая концентрация яда, которая в присутствии кефалина и хлорида кальция вызывает свертывание за 20—25 с; все ингредиенты берутся в количестве 0,1 мл и смешиваются) (таблица ниже).
С этой же целью используется препарат яда гадюки Расселла, обитающей в Индии (penyediaan стипвен).
Коагуляционные тесты, дифференцирующие дефицит факторов VII и X с помощью яда гюрзы (лебетокс) | |||
Дефицитные факторы в исследуемой плазме крови | Ujian | ||
с ядом гюрзы+кефалин+хлорид кальция | с ядом гюрзы+кефалин+хлорид кальция+профильтрованная плазма крови (источник факторов V а VIII) | протромбиновый | |
| Фактор X | – | – | – |
| Фактор VII | – | + | + |
| Nota kaki. (+) — нормализация свертывания; (-) — отсутствие нормализации свертывания. | |||
Дифференциальную диагностику завершают при необходимости количественным определением дефицитных факторов или их специфических иммунных ингибиторов, для чего применяются специальные высокочувствительные стандартизированные методики. В этих методиках используется построение кривых разведения смешанных образцов нормальной плазмы крови с коррекцией дефицита всех факторов, кроме исследуемого. По этим кривым определяется активность исследуемого фактора в плазме больных.
terutamanya важно количественное определение концентрации факторов VIII и IX, а также наличия их ингибиторов у больных гемофилией А и В (особенно до и во время хирургических вмешательств и при проведении интенсивной заместительной терапии), а также при отсроченных профузных послеродовых кровотечениях, когда приходится дифференцировать ДВС-синдром и более редкую патологию — появление иммунного ингибитора фактора VIII (еще намного реже — фактора V).
При глубоком дефиците фактора XIII (очень редкая наследственная патология) все коагуляционные пробы нормальны, но сгустки растворяются в 5М или 7М мочевине.
Помогает дифференцировать дефицит различных факторов свертывания также и учет степени и, terutamanya, сроков нормализации показаний тестов после внутривенного введения больным препаратов крови, t. ia adalah. учет коррекции di vivo по методике Л. 3. Баркагана.
Особенно эффективна эта методика при большой разнице продолжительности жизни дифференцируемых факторов в циркуляции. Sejak, продолжительность полужизни факторов протромбинового комплекса варьирует от нескольких часов (фактор VII) до нескольких дней (фактор II). Промежуточное положение между ними занимают факторы X (2—2,5 дня) и V (12—18 ч).
Поэтому после массивной струйной трансфузии плазмы протромбиновый индекс повышается при дефиците фактора VII очень кратковременно, при дефиците фактора V — несколько более длительно (примерно в 4—6 раз), а при дефиците факторов X и, terutamanya, II на более продолжительный срок (свыше 1—2 суток). Показательно в этом отношении и влияние на протромбиновый индекс препарата ППСБ (концентрата факторов VII, (IX), X и II). Он также кратковременно нормализует протромбиновое время при дефиците фактора VII и более длительно (во много раз!) при дефиците факторов X и II. Поскольку в этом препарате отсутствует фактор V, данный дефицит им не корригируется.
Аналогичное различие выявляется при трансфузионной и заместительной терапии факторов внутреннего механизма свертывания (XII, XI, IX и VIII), что регистрируется активированным парциальным тромбопластиновым тестом.
Особый интерес представляет динамика коррекции уровня фактора VIII и показаний АПТВ при трансфузионной терапии гемофилии А и болезни Виллебранда. При первом из этих заболеваний выявляется немедленное максимальное улучшение свертываемости после трансфузии (Jet, cepat!) антигемофильной плазмы или введения криопреципитата, а затем довольно быстрое (за 10—18 ч) неуклонное снижение ее, тогда как при болезни Виллебранда наблюдается некоторое нарастание свертывающей активности в течение нескольких часов после трансфузии, а затем ее снижение — намного более медленное, чем при. В связи с этим при лечении болезни Виллебранда более редко прибегают к заместительным трансфузиям, чем при гемофилии А.
Исследование функциональной активности факторов свертывания и компонентов калликреин-кининовой и фибринолитической систем с помощью хромогенных субстратов
Методы основаны на исследовании активности протеолитических ферментов и их ингибиторов, участвующих в свертывании крови, фибринолизе и образовании кининов, по интенсивности и скорости расщепления специфически чувствительных к этим ферментам пептидов, при деградации которых освобождается красящий агент (β-нитроанилин).
Степень окраски реагирующей смеси определяется спектрофотометрически, и по ее интенсивности судят об активности соответствующих ферментов (факторов свертывания, kallickreina, плазмина и др.), а по торможению процесса — об активности ингибиторов ферментов.
Sejak, sebagai contoh, действие гепарина и антитромбина III может быть оценено по ослаблению расщепления хромогенных субстратов фактором Xa или тромбином, а активность α2-антиплазмина — по ослаблению действия плазмина на соответствующий хромогенный субстрат. Хромогенные субстраты либо имеют цифровое обозначение (sebagai contoh, s-2222), либо именуются хромозинами с сокращенной приставкой, обозначающей тот фермент, к которому чувствителен этот субстрат (sebagai contoh, Chromozym PL — субстрат плазмина, Chromozym TH — субстрат тромбина, Chromozym PK — субстрат прекалликреина/калликреина и т. d.).
Хромогенные субстраты расширяют возможности исследования системы гемостаза, но пока недостаточно доступны для многих лабораторий. Некоторые исследования, выполненные с их помощью, не имеют преимуществ перед обычными коагуляционными тестами и дают совпадающие с ними результаты; в других случаях их использование упрощает и ускоряет исследование, делает его более точным; в третьих — эти методики имеют самостоятельное значение и не могут быть заменены коагуляционными тестами (sebagai contoh, определение прекалликреина).
Иммунологическое определение компонентов системы гемостаза
Иммунологическое определение компонентов системы гемостаза выполняется методами:
- Иммунопреципитации;
- Иммуноэлектрофореза;
- Радиоиммунологическими и другими с соответствующими антисыворотками
При этом оценивается содержание в плазме крови антигена того или иного фактора свертывания (или его фрагментов), а не функциональная активность, которая может быть резко сниженной при нормальном содержании антигена в плазме. Такая ситуация характерна для всех тех случаев, когда в организме синтезируются аномальные (функционально неполноценные) faktor-faktor, сохраняющие свою антигенность, но лишенные способности участвовать в гемостазе.
Это позволяет разграничивать полное прекращение синтеза соответствующих факторов и образование их аномальных форм.
Вместе с тем ряд компонентов системы гемостаза может определяться только иммунологически.
В эту группу входят такие важные исследования, как определение следующих компонентов:
- β-thromboglobulin;
- α2-макроглобулина;
- протеинов C и S;
- антигенов факторов VIII:C и VIII:Rcof;
- продуктов фибринолиза (Pdf);
- неоантигенов комплексов тромбин — антитромбин III и плазмин — антиплазмин;
- ряд других тестов.
Поэтому иммунологическое исследование существенно дополняет функциональную оценку разных звеньев системы гемостаза.
Ujian diagnostik, основанные на использовании в качестве реагентов препаратов из змеиных ядов
Давно установлено, что яды многих змей содержат высокоактивные протеолитические ферменты, вызывающие свертывание крови и воздействующие на разные звенья коагуляционного каскада. Вследствие этого змеиные яды и выделенные из них коагулазы широко используются для распознавания нарушений гемостаза, количественного определения факторов свертывания, выявления и количественного определения растворимых фибрин-мономерных комплексов (Rfmk) и ряда других исследований.
Пробы со змеиными ядами часто намного упрощают и делают более оперативной диагностику нарушений гемостаза.
В таблице приведены данные о механизме действия ядов на свертывающую систему крови и возможностях диагностического использования каждого из них.
Гемокоагулирующие свойства змеиных ядов и их использование в диагностической практике | |||
Наименование змей * и препаратов из их ядов | Механизм действия на свертывающую систему | Отличия от свойств естественных факторов свертывания | Возможности диагностического применения |
| Гюрза Vipera lebetina); лебетокс (гадюка Расселла; стипвен) | Активатор фактора X (в присутствии кальция, фактора V и фосфолипида **) | В отличие от тканевого тромбопластина не содержит фосфолипида и не компенсирует его дефицита. Не нуждается для реализации свертывания в факторе VII | Определение фактора и тромбоцитов и его освобождения при агрегации; разграничение дефицита факторов VII и X; количественное определение фактора X |
| Эфа многочешуйчатая (Echis multisgumatos) и эфа песчаная (Echis carinatus); экарин, эхитокс | Активатор фактора II, образует атипичный тромбин-Ем | В отличие от α-тромбина, тромбин-Ем не блокируется гепарином и антитромбином III, не активирует фактора XIII (сгустки лизируются в мочевине), коагулирует весь пул фибриногена и все растворимые комплексы фибрин-мономеров | Выявление гиперкоагуляции, в том числе скрытой, при лечении гепарином; количественное определение всего фибриногена и РФМК с целью диагностики тромбинемии и ДВС- sindrom |
| Щитомордник обыкновенный (Aghistrodon halus halus), а также многие гремучие змеи тропической Америки и Азии; анцистрон-Н1, рептилаза, ботропклотаза, кроталаза, анкрод и др. | Свертывает фибриноген, отщепляя только пептиды А и образуя неполные мономеры фибрина (дес-А-фибрин) | Не отщепляет пептиды В, Ia tidak mengaktifkan faktor XIII dan platelet, Ia tidak menyebabkan penarikan balik pembekuan, Ia tidak tersumbat dengan heparin, pembekuan cepat lyse | pengiktirafan disfibrinogenemy; оценка роли гепарина в нарушении конечного этапа свертывания (в сопоставлении с тромбиновым временем) |
| * Все указанные змеи обитают в Средней Азии (в скобках указаны другие виды со сходным механизмом действия и фирменные препараты из них; гадюка Расселла обитает в Индии, гадюка Дабойа — в Австралии. | |||
| ** Аналог кефалина и тромбоцитарного фактора 3. | |||
Эти возможности еще более расширяются при одновременном использовании нескольких ядов и простейших общих коагуляционных тестов. Sejak, sebagai contoh, одновременное применение коагуляционных проб с ядом гюрзы и эфы позволяет легко дифференцировать дефицит факторов VII, Х-V и II (в таблице ниже), а с дополнительной коррекцией профильтрованной нормальной плазмой (источник факторов V и II) —дефицит факторов X и V.
Коагуляционные тесты с применением различных ядов, дифференцирующие дефицит факторов протромбинового комплекса | |||
Дефицитные факторы в исследуемой плазме крови | Ujian | ||
с ядом гюрзы+кефалином | с ядом эфы | протромбиновый | |
| (VII) | + | + | – |
| X+V | – | + | – |
| II | – | – | – |
| Nota kaki. (+) — нормализация свертывания; (-)—отсутствие нормализации свертывания. | |||
Определение основных физиологических антикоагулянтов
Наиболее важное значение имеет определение активности основного физиологического антикоагулянта — антитромбина III, снижение которой может быть генетически обусловленным (первичная тромбофилия) либо вторичным вследствие интенсивного потребления (DIC, массивные тромбозы) или ускоренного метаболизма (лечение гепарином, L-аспарагиназой, синтетическими контрацептивными средствами) и блокады иммунными комплексами, парапротеинами, фибронектином, белками острой фазы.
В любом случае снижение активности антитромбина III ниже 60—65 % поддерживает внутрисосудистое свертывание крови, делает менее выраженным антикоагулянтное действие гепарина. Walau bagaimanapun, seringkali antara tahap antithrombin III dan menurun sensitiviti kepada heparin mempunyai pematuhan undang-undang-.
При этом обычно ослабление антикоагулянтного действия гепарина существенно преобладает над степенью снижения активности антитромбина III. Membuktikan, что при разных формах дефицита антитромбина III сродство его к гепарину может меняться в различной степени. Lebih-lebih lagi, разные фракции гепарина, соотношение которых в лекарственных средствах весьма изменчиво, также имеют различное сродство к антитромбину III. Поэтому практически важно исследовать как собственно активность антитромбина III, так и его способность превращаться под влиянием гепарина в быстродействующий антикоагулянт.
Антикоагулянтная активность антитромбина III
Антикоагулянтная активность антитромбина III определяется по способности исследуемой плазмы крови (разведенной — метод Копли—Винтерштейна или дефибринированной тепловой денатурацией при температуре 56 °С — методы Лолигера, Абильдгаарда и др.) инактивировать в течение определенного срока вводимый извне тромбин. Остаточная активность тромбина в такой плазме может определяться по ее свертывающей активности (на фибриногене, адсорбированной сульфатом бария плазме) либо по расщеплению хромогенного субстрата, чувствительного к тромбину или фактору Xa (поскольку антитромбин III инактивирует и этот фактор).
Гепарин-кофакторная активность
Гепарин-кофакторная активность содержащегося в плазме крови антитромбина III длительный период определялась с помощью теста толерантности плазмы к гепарину, который может считаться ориентировочным, поскольку дает очень большой разброс нормальных показателей и недостаточно воспроизводим.
Значительно более точны и воспро изводимы тесты, в которых исследуется влияние различных концентраций гепарина на тромбиновое время исследуемой плазмы, содержащей небольшое количество тромбоцитов. Сравнение проводится с удлинением тромбинового времени контрольной нормальной плазмы крови, к которой добавляются те же образцы гепарина.
Sejak, в тромбин-гепариновом тесте к исследуемой плазме крови добавляются такие количества гепарина, которые в контроле удлиняют тромбиновое время с 15 до 32—35 с (малая концентрация) и до 95—110 с (высокая концентрация гепарина). По этим данным рассчитываются индексы активности антитромбинов плазмы (ААП) и антикоагулянтного резерва плазмы (АРП).
Также широко используются сходные методики с оценкой степени инактивации тромбина как в коагуляционных тестах, так и на хромогенных субстратах.
Иммунологическое определение антигена антитромбина III
Иммунологическое определение антигена антитромбина III позволяет дифференцировать различные виды тромбофилии:
- с недостаточным синтезом антитромбина III (уровень антигенного маркера снижен адекватно снижению активности);
- с сохраненным синтезом аномальных и функционально неполноценных его форм (уровень антигенного маркера намного выше, чем активность).
Протеины C и S, тромбомодулин и α2-макроглобулин определяются иммуноэнзиматическими методами.
