Ganirelix – medikamentbeskrivelse
Når ATH:
H01CC01
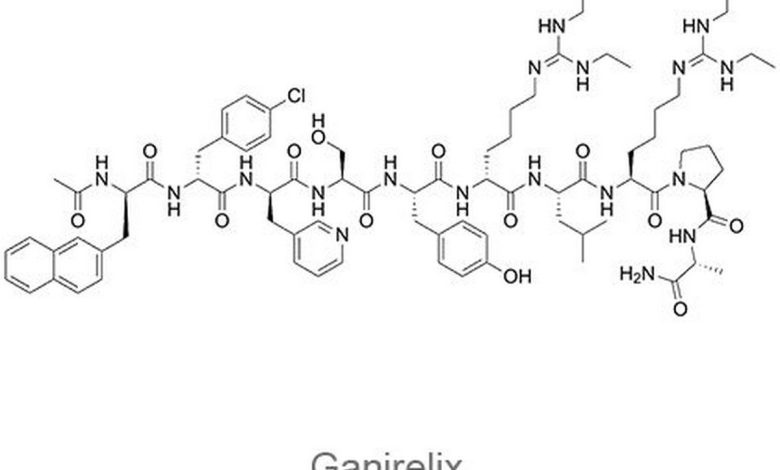
Ganirelix: karakteristisk
Gonadotropin-frigjørende hormonantagonist (GnRG). Syntetisk dekapeptid med høy antagonistisk aktivitet mot naturlig GnRH. Ganirelix acetat er et derivat av naturlig GnRH med aminosyresubstitusjoner i posisjoner 1, 2, 3, 6, 8 og 10. Løselig i vann.
Ganirelix: farmakologisk effekt
Antigonadotropnoe.
Ganirelix: søknad
Hemming av for tidlig topp-LH-sekresjon hos kvinner, gjennomgår kontrollert ovariehyperstimulering i infertilitetsbehandlingsprogrammer ved bruk av assistert reproduksjonsteknologi.
Ganirelix: Kontra
Overfølsomhet, inkl. til GnRH eller en hvilken som helst annen analog av GnRH, graviditet eller mistanke om graviditet.
Ganirelix: bruk under graviditet og amming
Kontraindisert ved graviditet eller mistenkt graviditet (Graviditet må utelukkes før behandlingsstart).
Med introduksjon av ganirelixacetat til drektige rotter og kaniner i perioden fra 7. dag til perioden nær levering i doser t.o.m. 10 og 30 mg / dag, henholdsvis (omtrent 0,4 og 3,2 ganger høyere dose for en person, basert på kroppen areal), det var en økning i prosentandelen av resorpsjon av avkommet. Det var ingen økning i fosterlidelser. Det var ingen medikamentrelaterte endringer i fertilitet, fysiske eller atferdsmessige egenskaper hos avkom av hunnrotter, behandlet med ganirelixacetat under graviditet og amming. Effekten på føtal resorpsjon er en konsekvens av endringer i hormonelle nivåer på grunn av stoffets antigonadotrope egenskaper., som kan føre til fostertap hos mennesker (bør ikke brukes til gravide kvinner).
Kategori handlinger resultere i FDA - X. (Dyreforsøk eller kliniske studier en krenkelse av fosteret og / eller det er tegn på risiko for skadevirkninger på menneskefostre, innhentet i forskning eller praksis; risiko, forbundet med bruk av narkotika i svangerskapet, større enn de potensielle fordeler.)
Kontraindisert under amming (ukjent, om HP i morsmelk).
Ganirelix: bivirkninger
Bivirkninger, som har blitt observert i fullførte kontrollerte kliniske studier siden den første dagen med bruk av ganirelixacetat (n=794) før bekreftelse av graviditet ved ultralyd hos ≥1 % av pasientene, brukte rusmidler, og var ikke direkte relatert til medisiner.
Magesmerter (gynekologisk) (4,8%), embryo/fosterdød (3,7%), hodepine (3,0%), ovarial hyperstimuleringssyndrom (2,4%), vaginal blødning (1,8%), reaksjoner på injeksjonsstedet (1,1%), kvalme (1,1%), magesmerter (gastrointestinale) (1,0%).
Sjeldne tilfeller av overfølsomhetsreaksjoner har blitt observert i studier etter markedsføring., inkludert anafylaktoide reaksjoner etter den første dosen.
Medfødte misdannelser
Ifølge resultatene av klinisk fullførte studier fra 283 Newborn, født av kvinner, ved bruk av ganirelixacetat, 3 hadde alvorlige medfødte anomalier (inkl. hydrocephalus / meningocele, omphalocele) og 18 - mindre alvorlige medfødte anomalier (inkl. nevus, hudmerker, sakral sinus, gemangioma, skjev hals / hodeskalle asymmetri, klumpfot, ekstra fingre, hoftesubluksasjon, torticollis/høy gane, navlebrokk, lyskebrokk, hydrocele, unedsatt testikkel, gidronefroz. En årsakssammenheng mellom disse medfødte anomaliene og bruken av ganirelixacetat er ikke identifisert..
Ganirelix: interaksjon
Bruk sammen med andre legemidler er ikke tilstrekkelig undersøkt, Muligheten for legemiddelinteraksjon kan derfor ikke utelukkes..
Ganirelix: Dosering og administrasjons
P /, 0,25 mg 1 en gang om dagen. Ganirelixacetat administreres vanligvis på den 6. dagen av FSH-preparatet (kontrollert stimulering av eggløsning med FSH begynner på 2. eller 3. dag i menstruasjonssyklusen). Bruken av stoffet bør fortsette daglig til den dagen du begynner å bruke hHC, dvs.. inntil dannelsen av et tilstrekkelig antall follikler av passende størrelse (preovulatoriske follikler) (bekreftet av ultralyd), da kan den endelige modningen av folliklene initieres ved administrering av hCG.
Ved økt eggstokkrespons på stimulering, for å forhindre for tidlig økning i LH-nivåer, behandling med ganirelixacetat bør begynne på dag 5 av FSH-administrasjon. Ved langsom vekst av follikler kan administreringen av ganirelix utsettes (dvs.. start senere enn 6. dag med bruk av FSH-preparater).
Det er nødvendig å avstå fra introduksjonen av hCG i tilfeller, hvis eggstokkene er for forstørret på siste dag av FSH-behandling (mulig utvikling av ovariehyperstimuleringssyndrom).
Ganirelix: forebyggende tiltak
Kan kun administreres av en spesialist, har erfaring med infertilitetsbehandling.
Sjeldne tilfeller av overfølsomhetsreaksjoner har blitt observert i studier etter markedsføring., inkludert anafylaktoide reaksjoner etter den første dosen (cm. «Bivirkninger av»).
Før du starter behandlingen, bør pasienten advares om behandlingens varighet., behovet for overvåkingsprosedyrer og risikoen for mulige bivirkninger. Behandlende lege skal informeres om medisiner, som pasienten tok kort før behandlingsstart eller fortsetter å ta parallelt med utnevnelsen av legemidlet.
Sikkerheten og effekten av legemidlet er ikke fastslått hos kvinner som veier mindre enn 50 kg eller mer 90 kg.
Med gjentatte behandlingsforløp bør stoffet kun brukes etter en grundig vurdering av graden av potensiell risiko og effektiviteten av behandlingen..
