貧血, グロビン鎖の構造の破壊に関連します
貧血, グロビン鎖の構造の破壊に関連します, haemoglobinopathies は病気のグループまたは, グロビン遺伝子の鎖の 1 つ以上のアミノ酸の交換のため, プロットやチェーンの欠如 それを長くすることで.
ヘモグロビン症の臨床像 置換の場所によって異なります. ヘモグロビン症は貧血として現れることがある, 血液に変化を与えたり、ヘモグロビンや赤血球の含有量を増加させたりしないこと.
構造が変化したヘモグロビンの最初の説明は、 1949 街, いつ発見されましたか, 鎌状赤血球貧血のヘモグロビン, アルカリ性媒体中で電気泳動中に高速で移動すること, 少ない, 大人のヘモグロビンよりも.
IN 1956 d ペプチドマップ法を使用した場合に確立された, ヘモグロビンとは何ですか, 鎌状赤血球症で発見され、 ヘモグロビンS, β鎖のたった1つのアミノ酸の変化により、健康な人のヘモグロビンAと異なります。. 通常、グルタミン酸はβ鎖のN末端から6番目に位置します。, ヘモグロビン症 S - アミノ酸バリンの場合. グルタミン酸とは担当が異なります, ヘモグロビンは、したがって、より低い速度で電場に移動します.
ほとんどの異常ヘモグロビン症は、ヘテロ接合のいずれかの臨床症状を提供しません, ホモ接合状態のいずれかで. なお、これらの場合に観察されます, アミノ酸置換は、ヘモグロビンおよびヘモグロビンの三次または四次構造を破壊しない場合には基本的な機能が保存されています. 一部の異常ヘモグロビンはホモ接合状態又はサラセミアと組み合わせた臨床症状を提供します. 異常な不安定ヘモグロビンのグループの存在下で、病理学的遺伝子のヘテロ接合保因者に疾患の臨床徴候が見つかることがあります。. これらのヘモグロビン症では、置換は機能的に最も重要なアミノ酸に関係します. これらのアミノ酸は、グロビンへのヘムの固定に関与しています。, グロビン鎖同士の結合.
Serpovidnokletochnaya貧血, ヘモグロビン症 S, Cはアフリカのさまざまな国に蔓延しています. ヘモグロビン症の一般的な形態にはヘモグロビン症 E も含まれます, Dペンジャブ.β鎖のアミノ酸置換ははるかに一般的です, αチェーンよりも.
異常なヘモグロビンを特定するには、まず患者の体内にそのヘモグロビンが存在することを確認する必要があります。. 酢酸セルロースフィルム上の電気泳動によりヘモグロビンSおよび安定型ヘモグロビンを検出, 紙. しかし、電気泳動の研究では、 1/3 異常なヘモグロビンの一部. 貧血に, グロビン鎖の構造の破壊に関連する, ヘモグロビン症の診断は、ヘモグロビンの不安定性の兆候が検出された場合にのみ行われます。, 電気泳動移動度に変化がない場合が多い.
異常ヘモグロビンの兆候を特定した後、何らかの方法でヘモグロビンを分離する必要があります。 (電気泳動, 熱変性, クロマトグラフィー) 正常なヘモグロビンAから, 連鎖の解明, 置換が行われる場所 (連鎖加水分解法, それらの電気泳動またはクロマトグラフィーによる分離).
次のステップは、異常鎖のトリプシン加水分解です。, ペプチド精製のためのペプチドマップの取得, 異常があるところ, 病理学的ペプチドのアミノ酸組成の研究, 必要に応じて、ペプチド内のアミノ酸の順序を研究します。.
ヘモグロビンを表す場合、その名前に加えて、鎖が与えられます。, 置換が行われる場所, 鎖内のアミノ酸の数を示します (窒素端から始まる), アミノ酸名, この場所にあるのは, そしてアミノ酸の名前も, このエリアにあるはずだったもの. 例えば, ヘモグロビンEα2B226グル→ブァル 手段, 私たちが話しているのはヘモグロビン症 E についてです, β鎖の26番目のアミノ酸であるグルタミン酸がバリンに置き換わったもの.
貧血, ヘモグロビンの運搬が原因, 低酸素状態での構造を変更します
ヘモグロビン構造の最も一般的な異常はヘモグロビン異常症 Sα です2B26グル→ブァル. ホモ接合型保菌の場合、鎌状赤血球貧血について話します。, ヘテロ接合体 - 鎌状赤血球異常について.
Drepanocytemia アフリカ諸国で蔓延している (アンゴラ, モザンビーク, コンゴ, リベリア, アルジェリア, チュニジアなど). この病気はインドでよく見られます。, セイロン島で, トルコで, イラン, イラク, キューバへ.
シックリング現象 ヘモグロビンの溶解度の低下の結果です, 酸素を放棄した, ヘモグロビンAと比較して. ヘモグロビンA, 酸素が欠乏した, 2倍に溶かす, ヘモグロビンAよりも, 酸素化された. 酸素の放出に伴うヘモグロビンSの溶解度は、 100 時間. これによりゲルが形成されます. 顕微鏡検査により、結晶の大きさが明らかになります 1,5 M, 鎌状の赤血球. クリスタル, 一方向に成長する, と呼ばれます タクトイド. ヘモグロビンに酸素が加わると消えます. これは、想定することができます, このような場合、6位のグルタミン酸をバリンに置き換えると、あるヘモグロビン分子と別のヘモグロビン分子の結合が増加する, ヘモグロビン分子に酸素が結合していないとき. これにより、分子の溶解度が低くなります。. 赤血球中のヘモグロビンCの存在, Dペンジャブ, 〇アラブ 鎌状赤み現象を増加させる, 一方、ヘモグロビン P が大量に存在すると、赤血球の鎌状赤血球の程度が減少します。.
ヘモグロビン症 S のホモ接合型 (drepanocytemia)
臨床的には中等度の正色素性貧血を特徴とする, 血管血栓症, 特殊なタイプの患者. この病気の最初の症状は、子供の誕生からわずか数か月後に現れます。, 胎児ヘモグロビン以来, 出生時の初等, 病的なβ鎖を含まず、損傷を受けない. ほかに, 病理学的連鎖の発症後の幼児における胎児ヘモグロビンの高レベルは、酸素に対する親和性の増加により鎌状赤血球の現象を軽減します.
幼児期の鎌状赤血球貧血の最も特徴的な症状は、骨と関節の損傷です。.
肺梗塞は、肺血管の血栓症が原因で小児に多く観察されます。. このプロセスの進行には、体温の高い数値の上昇が伴う場合があります。, 白血球数の増加. 腎梗塞の発症の可能性.
時々、関節や肺のプロセスの悪化の期間中に、子供は黒い尿を伴う血管内溶血の現象を伴う重度の溶血性危機を発症します。, ヘモグロビンレベルの急激な低下を伴う, 高熱. 高齢になると、これらの現象は重度の腹痛を伴うことがよくあります。, この病気の血栓性合併症に関連する.
硝子体出血や網膜剥離は失明の原因となることが多い.
神経系への損傷は血管血栓症によっても引き起こされる可能性があります, 脳のさまざまな部分に栄養を与える.
幼児期に脾臓が肥大する, その後は減少します, 以降 5 数年間、脾腫はほとんど観察されません. これは鎌状赤血球貧血の特徴的な症状である自己脾摘出術によるものです。, 頻繁な梗塞の結果として起こる脾臓の線維化によって引き起こされる. 肝臓が肥大することが最も多い.
成人の場合, 鎌状赤血球貧血に苦しんでいる, 時々観察される 持続勃起症, 接続された, 最も可能性が高いです, 海綿体の鎌状赤血球の停滞を伴う, 何, 順番, 低酸素と鎌状赤血球の形成を増加させます.
血液検査の結果、軽症であることが判明 正色素性貧血: ヘモグロビン含有量 3.72-4.96 mmol/l (60 - 80 G / L). 染色塗抹標本では、鎌状の赤血球が現れることがあります。, ただし、赤血球の好塩基性点状の存在はより典型的です。, ターゲティング. 鎌状赤血球は、メタ重硫酸ナトリウム検査を使用するか、指の付け根に止血帯を適用することによって検出できます。.
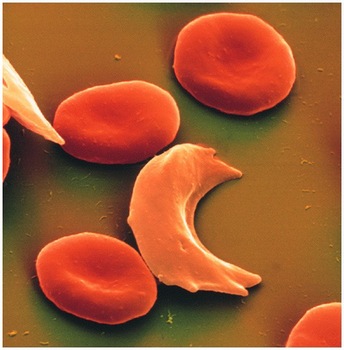
網状赤血球の内容, 骨髄赤核球の数と間接ビリルビンのレベルが増加します。, ESR はほとんどの場合正常範囲内です, 鎌状赤血球の定着が遅いため, 通常より.
起こり得る隔離危機, 内臓の赤血球のかなりの部分が消失する状態. これは崩壊の発症につながる可能性があります, 迅速な輸血が必要な除去の場合.
記載 再生不能の危機, 重度の貧血が発症する場合, 白血球減少症, 網赤血球が消える. ほとんどの場合、重度のウイルス感染後に発生します。.
鎌状赤血球症患者のほとんどは幼児期に死亡します. 妊婦の死亡率は非常に高い, 鎌状赤血球貧血に苦しんでいる. いくつかの報告によると、, 鎌状赤血球形成不全による妊産婦死亡率は次のとおりです。 6 %.
ヘモグロビン症 S のヘテロ接合型 (鎌状赤血球異常)
この形態のヘモグロビン症では、患者は自分の病気に気づいていないことがあります。, 彼らのヘモグロビンレベルは正常です, 満足のいく状態. 一部の患者におけるこの病気の唯一の症状は血尿です, 小さな腎血管梗塞と関連がある. ヘテロ接合型ヘモグロビン症患者の赤血球中の異常ヘモグロビンの含有量は低い, 病気の臨床症状は低酸素状態のときにのみ観察されます。, 重度の肺炎の場合, 麻酔中, 減圧された航空機で飛行する場合.
血栓症の症状 どの臓器でも発生する可能性があります, 鎌状赤血球貧血でその病変が観察される. シックリング現象はメタ重硫酸塩検査を使用して患者で検出される. ヘモグロビン電気泳動により、ヘモグロビン A とヘモグロビン S という 2 つの大きな画分が明らかになります.
ヘモグロビン症 S のヘテロ接合型の合併 (鎌状赤血球症) β-サラセミアを伴う.
頻繁に発生する, よりスムーズに動作します, ホモ接合性β-サラセミアおよびホモ接合性ヘモグロビン症Sよりも.
脾臓の顕著な肥大を特徴とする, 赤血球の重度の色素欠乏症, 高いターゲット可能性. 血栓性合併症が観察される頻度ははるかに低くなります, 鎌状赤血球貧血よりも. 関節痛の発作の可能性, 胃. 身体の発育に遅れがある. 胎児ヘモグロビンのレベルの有意な増加によって特徴づけ. 電気泳動ではヘモグロビン A が検出されない, そしてヘモグロビンSはほぼ唯一のヘモグロビンである可能性があります. Hb Sに加えてβ-サラセミアに対して, あ2 胎児ヘモグロビンAが検出される.
ヘモグロビンFの含有量が高いと、シックリング現象がはっきりと現れません.
貧血, 安定した異常ヘモグロビンの保持によって引き起こされる
このような貧血の最も一般的な形態はヘモグロビン症 C です。, Dペンジャブ иE.
これらすべてのタイプのヘモグロビン症は、ヘテロ接合状態にあり、相互に組み合わされたり、サラセミアと組み合わされたりしても、臨床症状を呈しません。. ホモ接合性ヘモグロビン症 C では、脾臓の肥大と消化不良の症状を伴う軽度の溶血性貧血が検出されます。. 塗抹標本中にターゲット形状の赤血球が検出される. ヘモグロビン症Dの場合ペンジャブ ホモ接合状態では非常にまれです, ホモ接合状態のヘモグロビン症 E では、軽度の溶血性貧血が検出されます。, 脾臓のわずかな肥大. 3 種類のヘモグロビン症とサラセミアが組み合わさると、臨床像がより重篤になり、脾臓の顕著な腫大が引き起こされます。.
これら 3 種類のヘモグロビンはすべて、β 鎖の置換によって特徴付けられます。. ヘモグロビンCでは、グルタミン酸の6番目のユニットがリジンに置き換えられます。, ヘモグロビンEのグルタミン酸の26番目の単位はリジンです, ヘモグロビンDではペンジャブ 121-グルタミン酸の単位 - グルタミン.
ヘモグロビンDの移動度ペンジャブ ヘモグロビンSの移動度に相当, ただし、ヘモグロビン症 S とは異なり、ヘモグロビン症 Dペンジャブ 溶解性とシックリングの検査は正常であることが判明. ヘモグロビンEの移動度は同じ, ヘモグロビンAの移動性と同様に2, しかしヘモグロビンAの量は2 こんなことは決してない, ヘモグロビン症 E と同様.
この病気は西アフリカで発生します, 七面鳥, イラン, インド (パンジャーブ州).
ヘモグロビン症Eがインドで発生, カンボジア, ビルマ, インドネシア.
貧血, 不安定な異常ヘモグロビンの保持によって引き起こされる
不安定ヘモグロビンとは、このような異常なヘモグロビンのことを指します。, 分子の不安定性により、赤血球内で沈殿します。, これは、病理学的遺伝子のヘテロ接合保因者における溶血性貧血の発症につながります。.
病因と病理発生
IN 1952 G. キャシーさんは先天性溶血性貧血を患う子供について語った, この患者では、脾臓摘出後にすべての赤血球にハインツ小体が検出されました。. 後ほど 18 年が確立されています, これらの体の出現の原因はヘモグロビンの異常な割合であるということ. 当初、このグループの疾患はハインツ小体を伴う先天性溶血性貧血と呼ばれていました。.
確立された構造を持つ最初の不安定なヘモグロビンは Hb でしたチューリッヒ, で発見された 1962 G. 二人の患者で, サルファ剤の服用後に急性溶血性危機を経験した人.
研究により判明したのは, ハインツ小体の患者のヘモグロビンの一部は、わずかな加熱で容易に沈殿する. IN 1969 G. このグループの病気に対して新しい名前が提案されました - 溶血性貧血, 不安定なヘモグロビンの運搬によって引き起こされる.
このタイプの貧血は優性遺伝します。. ヘモグロビン分子の不安定性が検出される場合, アミノ酸置換がグロビンとヘムの結合に影響を与える場合, 接続α- およびグロビンのβ鎖同士, アミノ酸置換が起こった場合も, ヘモグロビンヘリックスに含まれる, アミノ酸プロリン, 特殊な構造のため、螺旋に入り込むことができません。.
ヘモグロビン分子の不安定性が検出される場合もあります, グロビン分子の一部の場合, ヘムが隣接しているもの, いわゆるヘムポケットの中に, 非極性アミノ酸 (グリシン, バリン, アラニンなど。) 極に置き換えられました (グルタミン, アスパラギン酸など。). この場合、水分子はヘムポケットに侵入します。, ヘモグロビン分子の安定性を破壊する.
ヘモグロビンの不安定性 1 つ以上のアミノ酸の欠失またはサブユニットの伸長が原因である可能性もあります. これはヘモグロビン分子の変形とその安定性の破壊につながります。. その結果、ヘモグロビン症の一部の形態では、赤血球内に複数の封入体が出現します。, 不安定なヘモグロビンの沈殿によって引き起こされる. 他の場合には、単一のハインツ小体が赤血球内に見出されます。, いずれかのヘモグロビンを表す, ヘム欠損, または単離されたグロビン鎖の沈殿.
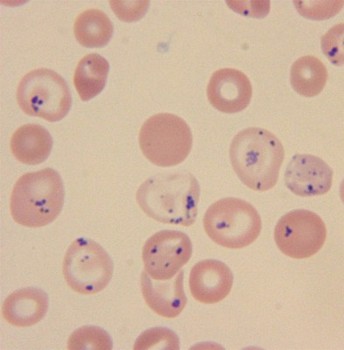
臨床症状
貧血の臨床症状は多様であり、アミノ酸置換の位置によって異なります。.
ヘモグロビン値が正常な患者もいます, 他の場合では、2.48-3.72 mmol/l に減少します。 (40-60 G / L). 重度の疾患または中等度の溶血性貧血の場合、臨床症状は小児期からすでに観察されています。. 黄ばみの程度, 貧血の程度も, アミノ酸置換の性質によって異なります: 一部の患者では、皮膚と強膜の色は正常です, 持続的または断続的な重度の黄疸を患う人もいます. ほとんどの患者で脾臓が肥大している, ただし、ヘモグロビン症の一部の形態では正常のままです。. 肝臓肥大の可能性. この貧血は胆石症を合併することがよくあります. 骨格の変化も同じかもしれない, microspherocytosisのように, 軽度の貧血ではそれらは存在しません.
検査所見
不安定なヘモグロビンを運ぶと、さまざまな重症度の貧血が検出されます, 多くの場合、正色素性, 時々淡色, ヘモグロビンの一部が沈殿するため, 特に場合には, ヘムがグロビンから切断される場合、または沈殿物が別個の鎖で構成される場合. 標的赤血球を検出, 赤血球不同症, polihromaziya. 網赤血球の含有量は常に増加します. 骨髄の赤い芽の刺激がある.
ヘモグロビン症の血液像と臨床症状 アミノ酸置換の性質のみに依存する. 患者における同じヘモグロビン症, 無関係の異常ヘモグロビン保有者が同じ臨床症状を示す. そう, ヘモグロビン症用 Biba, サバンナ, キャスパー, 重度の溶血性貧血のヴォルガクリニックが観察される, ヘモグロビン症用 タコマ, ベルファスト, キャスパー, モスクワでは最小限の臨床症状がある. 一部のヘモグロビン症では、酸素に対する親和性が変化します.
酸素に対するヘモグロビンの親和性が増加したヘモグロビン症のほとんどは、α-α間の接触におけるアミノ酸の置換を特徴としています。- そしてβ鎖 (A1B2-連絡先). 酸素親和性の増加はアミノ酸置換にも関連している可能性があります, 2,3-ジホスホグリセリン酸 - 物質の結合に関連する, ヘモグロビンによる組織への酸素の正常な放出に必要. ヘモグロビン症の場合, 酸素に対する親和性の増加に関連する, 組織の低酸素状態により、赤血球増加が観察される場合があります, 貧血ではない. どこ, 酸素親和性が低下すると, 貧血が起こる可能性がある, 溶血の増加が原因ではない, そして高酸素症. このような場合、本質的に溶血性ではありません, aはエリスロポエチンレベルの低下と関連しています.
ヘモグロビン症の診断
ヘモグロビン症の診断, 不安定な異常グロビンの保持によって引き起こされる, それに基づいて、, 赤血球がさまざまな酸化剤にさらされると, 明るいクレシルブルーなど, 不安定なヘモグロビンの一部は変性を受け、小さな複数の封入体の形で沈殿します。.
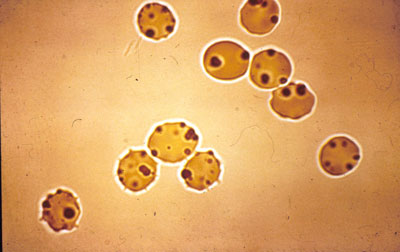
同じ封入体がヘモグロビン症 H にも見られます。, そんなふうに, モスクワ. この染色は、網赤血球の含有量を測定するために一般的に使用されます。. インクルージョンを明確に識別するには、以上のものをインキュベートします。 2 いいえ.
多くの患者では、酸化的に汚れた場合、, および非酸化染料 (例えば, クリスタルバイオレット) 赤血球中に単一の大きなハインツ小体が検出される, 偏った位置にある. ほとんどの場合、それらは患者に観察されます, 脾臓摘出手術を受けた人.
ヘモグロビンの熱不安定性を調べる方法 それはこの中にあります, 加熱条件下では 55 pHで°C 7,4 で 0,15 M リン酸緩衝液は正常です 1 h は平均して約約 13 % ヘモグロビン, 不安定なヘモグロビンの存在下 - 詳細 25 %.
不安定なヘモグロビンを検出する高速メソッド, 以下のようになります. 血液溶血物が入れられます 17 % トリス緩衝液中のイソプロピルアルコールの溶液および一定温度でインキュベート 37 °C. 不安定なヘモグロビンが存在すると、5 ~ 15 分以内に沈殿が形成されます。, 通常、それは30〜40分後にのみ現れますが、.
試薬: 17% ソリューションイソプロ- でアルコールを飲む 0,1 M緩衝液, トリス塩酸 (pH値 7,4). 溶液は密閉容器に入れれば長期保存可能.
メソッド. 溶血物, およそを含む 6,21 ミリモル/リットル (100 G / L) ヘモグロビン, 1~1.5倍量の蒸留水を加えて等張塩化ナトリウム溶液で3回洗浄した赤血球から調製. 赤血球は振ることで溶血します, 脂質は、半分の量の四塩化炭素を用いて振盪することにより抽出されます。 2 M. 遠心分離後 10 分で 3000 rpm トップ層は研究のために分離されています.
イソプロピルアルコール溶液を注ぎます。 2 ミリリットル 2 試験管, ストッパーで閉まる. 試験管はある温度で加熱されます 37 ウォーターバス内で °C. いずれかの試験管に注ぎます 0,2 溶血液 ml, 患者の赤血球から得られる, 別の人に - 0,2 溶血液 ml, ドナーの赤血球から得られる. 不安定なヘモグロビンが存在すると、5 ~ 15 分以内に沈殿が形成されます。. 誤った結果が生じる可能性もあります。. 不正確な場合, アルコール濃度が高い, 試験管を加熱するときの温度が高くなる, pHがより酸性になると、正常なヘモグロビンがより早く沈殿する可能性があります 30 M. メトヘモグロビンの濃度が高い場合、オキシヘモグロビンと比較してメトヘモグロビンの安定性が低いため、沈殿物が現れる場合があります。.
この方法を使用してヘモグロビンの安定性を研究するには、新鮮な溶血液のみを使用する必要があります. この場合、考慮する必要があるのは、, ヘモグロビン濃度が近いはずです 100 G / L.
現在、不安定なヘモグロビンを検出するには、β-安息香酸水銀またはβ-クロロ安息香酸水銀による処理とそれに続くデンプンゲル電気泳動が使用されています。.
IN 1981 G. 不安定ヘモグロビンを測定するための新しい方法が高速法として提案されました, それに基づいて, 低濃度の亜鉛塩が存在すると、ある温度で不安定なヘモグロビンが沈殿すること 37 ℃ 15 正常なヘモグロビンとは対照的に最小. この場合、溶血量は 0,2 ミリリットル (6,21 ミリモル/リットル, または 100 g/lヘモグロビン) ソリューションに追加されました, 含む 0,35 ミリリットル 0,003 M酢酸亜鉛溶液と 1,45 ミリリットル 0,1 M トリス緩衝液 (pH) 7,4. 混合後、試験管をサーモスタットに入れ、 30 分で 37 °C. 不安定なヘモグロビンが存在すると、すぐに沈殿が生じます。, 解決する 30 M.
一部のヘモグロビン症の場合、血液を 1 ~ 2 日間予備培養した後, そして時々、新鮮な血液ではメトヘモグロビン含有量が増加します.
電気泳動による移動度による (紙や酢酸セルロースで研究する場合) 既知の不安定ヘモグロビンの 3 分の 1 のみがヘモグロビン A と異なります. 場合によっては、デンプンまたはポリアクリルアミドゲル上の電気泳動移動度の変化を検出できる場合があります。. 不安定なヘモグロビンの一次構造を研究することで、その種類を正確に判断できるようになります。.
