Interazioni farmacocinetiche e concetti generali di equivalenza e biodisponibilità dei farmaci
Sviluppare approcci comuni uso di stupefacenti farmacoterapia specifiche, deve essere considerato, che i diversi tipi di forme di dosaggio hanno diverse biodisponibilità. Se l'assorbimento sostanza medicinale dipende essenzialmente dalle sue proprietà fisico-chimiche, la biodisponibilità - largamente dalle proprietà della formulazione. In relazione a questo importante importanza clinica è il concetto di equivalenza, e la biodisponibilità di farmaci.
Farmaceutico (chimico) equivalenza Medicina mezzi, contengono la stessa quantità di principio attivo e sono conformi agli standard esistenti, mentre i loro ingredienti inattivi possono variare.
Il concetto di bioequivalenza Si riferisce ad una preparati chimicamente equivalenti, che quando somministrato a un paziente alle stesse dosi e lo stesso schema nel sangue e nei tessuti del composto attivo si accumula in concentrazioni uguali.
Il concetto di equivalenza terapeutica Si riferisce ai farmaci, che, quando somministrato ad un paziente in dosi uguali e lo stesso modello presentano sostanzialmente la stessa efficacia terapeutica o tossicità; mentre questi farmaci possono essere nebioekvivalentnymi.
L'idea dell'efficacia del farmaco è sempre stata associata con essa biodisponibilità. Caratteristica Quantitative, determinazione della biodisponibilità dei farmaci (per definizione FDA), è la velocità e l'entità di accumulo del farmaco a loro azione prevista. Tuttavia, per ottenere campioni di tessuto e li esaminerà per i contenuti di droga impossibile nell'esperimento. Pertanto la biodisponibilità della sostanza farmaco è giudicata dalla sua concentrazione nel sangue. In pratica, determinare la biodisponibilità assoluta e relativa.
La biodisponibilità assoluta È l'atteggiamento (in %) la quantità di farmaco è cresciuta profonda, somministrati in una forma di dosaggio orale o altro, al numero di vsosavshegosya
stessa sostanza, nella stessa dose, ma come infusione endovenosa o iniezione, fornitura 100% biodisponibilità.
Biodisponibilità relativa del farmaco Può essere misurata confrontando l'area sotto la curva concentrazione-tempo, caratterizzante la concentrazione della sostanza nel siero di entrambi i farmaci nel metodo identico di somministrazione, ad esempio per via orale o rettale. La biodisponibilità è valutata la concentrazione del farmaco nel sangue o nelle urine, se la sostanza è escreta in tal quali.
Se farmaci hanno la stessa biodisponibilità in condizioni identiche, sono considerati bioequivalenti.
Secondo la FDA, preparazioni possono essere bioequivalente, nonostante le differenze nella velocità e l'entità dell'assorbimento (quando il tasso di assorbimento non è caratteristica critica per ottenere la concentrazione effettiva della sostanza attiva nel corpo o è irrilevante per la manifestazione dell'effetto terapeutico del farmaco). In alcuni casi, la velocità di assorbimento del principio attivo di farmaci possono influenzare l'efficacia del trattamento. Un lato, con lenta concentrazione della sostanza di assorbimento nel sangue può essere inferiore alla minima terapeutica, che non prevede l'effetto terapeutico desiderato, e dall'altro - a troppo rapido assorbimento, essa può notevolmente superare la soglia di concentrazione ammissibile, provocare effetti collaterali indesiderati, o tossiche. Pertanto, i farmaci, caratterizzato da una leggera differenza tra le minime dosi tollerate efficaci e massimo della sostanza, sono bioequivalenti se, e se il grado di, e la velocità di aspirazione sarà identica.
Il problema è particolarmente acuto biodisponibilità, quando i farmaci sono destinati alla somministrazione orale. Dal punto di vista clinico Pharmacy importante differenza nella biodisponibilità di sostanze provenienti da diversi tipi di forme di dosaggio. La sua definizione è ostacolato dalla incapacità di tenere conto di tutte le caratteristiche individuali del paziente e le diverse proprietà delle forme di dosaggio. Quando assunti per via orale, la preparazione della droga, prima di raggiungere la circolazione sistemica, Subisce un numero di transizioni e di destinazione raggiunge meno, che provoca una bassa biodisponibilità (ad esempio,, norepinefrina, Testosterone, fenacetina et al.). Le ragioni della bassa biodisponibilità della sostanza può essere insufficiente durante la sua permanenza nel tratto digestivo, così come l'età, sesso e differenze geneticamente determinate, diverso paziente attivo, la presenza di situazioni di stress, la presenza di alcune malattie, etc.. d. Biodisponibilità diminuisce sostanze e sotto l'azione di molteplici fattori, che interessano il suo assorbimento.
Problemi particolari sorgono quando la terapia a lungo termine, quando il paziente, è atta ad un tipo di forma di dosaggio, trasferita ad un'altra, Non equivalenti. In questo caso, può ridurre l'efficacia della terapia, Si verificano effetti tossici. Tali casi sono noti quando si cambia la droga digossina, fenitoina, ecc.
A volte è possibile ottenere l'equivalenza terapeutica di farmaci, Nonostante le differenze nella loro biodisponibilità. Per Esempio, la differenza tra le concentrazioni terapeutiche e tossiche di penicillina alta, pertanto fluttuazioni sua concentrazione nel sangue, a causa della variazione della biodisponibilità di farmaci, non possono influenzare in modo significativo la loro efficacia terapeutica e la sicurezza. Opposto, per i farmaci con una relativamente piccola differenza tra il terapeutico e la differenza di concentrazione tossica nella biodisponibilità è importante.
Poiché l'effetto terapeutico, la durata e l'intensità tempo dipendenza è causato dalla concentrazione del farmaco nel plasma sanguigno, di solito prendere in considerazione tre opzioni - la concentrazione massima di una sostanza nel sangue, il tempo per raggiungere, e l'area sotto la curva, conseguente le coordinate del tempo-concentrazione.
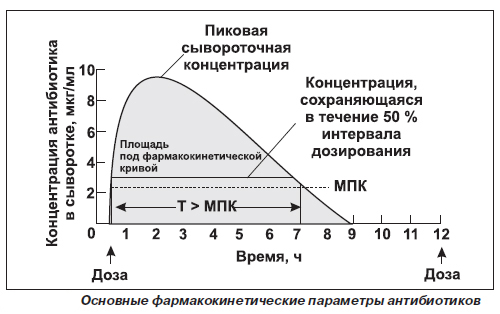
Gli spettacoli figura, che la concentrazione della sostanza nel sangue aumenta con la velocità e l'entità dei suoi picchi di assorbimento e, quando il tasso di materiale dal corpo diventa uguale al tasso di assorbimento. L'assorbimento lento della sostanza, il successivo raggiunge la sua concentrazione massima.
Tuttavia, una biodisponibilità stima basata sui dati di massima concentrazione di droga nel sangue non può essere sufficientemente accurata, poiché la ricezione della sostanza nella circolazione sistemica inizia la sua eliminazione. Il tempo per raggiungere la massima concentrazione dipende dalla velocità di agente di assorbimento e un indicatore del tasso. La misura più importante è l'area sotto la curva della concentrazione biodisponibilità (PKK) di volta. Esso è direttamente proporzionale al contenuto totale di sostanza invariata nel plasma sanguigno. Per determinare il PKK effettuato il prelievo di sangue per l'eliminazione totale di una sostanza. Due medicinali, avendo identico tasso di curve e il grado di assorbimento può essere considerato bioequivalente. Se i farmaci hanno la stessa PAC, ma differiscono nelle forme delle curve di concentrazione vs. tempo, essi sono considerati equivalenti in grado di assorbimento, ma differiscono nella sua velocità.
Determinazione della biodisponibilità ripetuta somministrazione del farmaco è preferito. PAC è misurata in uno degli intervalli tra due amministrazioni consecutive. I risultati più accurati vengono mediate nel determinare biodisponibilità entro giorni. Se il farmaco viene escreto nelle urine (principalmente in forma invariata), la biodisponibilità può essere valutata, determinare l'importo totale per il momento, uguale 7-10 emivita della sostanza. Una definizione più precisa della biodisponibilità possibile lo studio del sangue e urine contemporaneamente.
Quindi, biodisponibilità e la bioequivalenza sono gli indicatori più importanti della qualità dei farmaci nella caratterizzazione delle loro opzioni terapeutiche.
