藥物的作用機制
在大多數情況下,, 藥物 (配體) 它有它的效果, 它必須滿足人體的特定組件 - 靶受體, 分子結構, 代表 是蛋白質, 不太常見的核酸, 脂質或其他構型, 位於細胞內部或表面, 它與誰相互作用, 啟動一系列生化和物理化學過程, 從而達到一定的效果.
膜受體有兩種類型:離子通道和受體, G蛋白偶聯. 例如, 乙酰膽鹼和類似藥物的特點是鈉通道. 乙酰膽鹼與通道蛋白相互作用, 引起其構象變化, 促進通道的開放和鈉離子滲入細胞. 這個過程是神經興奮的基礎. 有些藥物, 與鈉通道蛋白相互作用, 阻止它打開, 從而阻斷神經興奮的傳遞.
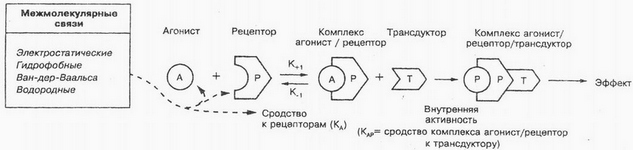
所謂的 G 蛋白附著在細胞質膜的內部。, 確保藥物相互作用過程與相應細胞內靶蛋白的同時激活同步. 如圖所示, 藥物分子與受體相互作用 (P) 在膜的外表面, 導致受體蛋白構象變化. 因此,G 蛋白改變了其空間結構, 在膜平面內遷移至酶, 它們在細胞內處於非活性狀態. G 蛋白與酶的相互作用 (Ť) 導致它們的激活 (左/左/右). 去甲腎上腺素, 多巴胺和其他配體與受體特異性相互作用, G蛋白偶聯. 需要注意的是, 乙酰膽鹼不僅可以與通道蛋白相互作用, 但也與受體, G蛋白偶聯.
為了發生配體和生物受體之間的相互作用,必須, 使它們具有互補性, 也就是說,他們之間必須有一定的親和力, 或親和力 (尺寸匹配, 空間配置, 相反電荷的存在等. D。). 例如, 外源配體的正電荷必須與受體的負電荷相對應, 物質的非極性基團可以與受體的疏水區域結合.
藥用物質的理化性質, 影響它們與受體的相互作用, 應突出顯示分子的大小, 取決於該物質可以與整個受體或其成分相互作用. 其滲透生物膜的動力學還取決於藥物分子的大小。. 通常,隨著分子尺寸的增加,其靈活性以及與大分子夥伴形成范德華鍵的可能性也會增加。. 除了, 藥物分子的立體化學很重要. 從, 該藥物的異構體形式是什麼?, 取決於其藥理活性. 你需要記住: 受體分子的構象越剛性, 立體異構體效果差異越大.
藥物-受體相互作用通過分子間鍵發生. 最初,利用靜電力將物質吸引到受體上, 在存在互補性的情況下,它利用物理和物理化學相互作用與受體形成鍵 (典型的藥用物質, 從體內排出時未發生變化或幾乎沒有變化) 或化學相互作用 (內在的聯繫, 在體內發生化學變化). 最弱的范德華力參與確定藥物與生化反應系統相互作用的特異性. 氫鍵參與物質的識別和固定過程 (配體的) 生物結構. 離子鍵發生時, 當藥物含有陽離子或陰離子基團時, 相反的結構位於生物受體中. 離子鍵通常在物質和受體之間藥理反應的第一階段形成. 在這種情況下,藥物的作用是可逆的. 配位共價鍵的形成很重要. 在它們的參與下,烷化劑與生物底物發生相互作用, 以及與金屬形成穩定螯合物的藥物和解毒劑, 例如:, 單位硫醇與砷或茶鹼鈣與鉛. 此類物質的影響是不可逆轉的.
除了, 存在疏水相互作用. 雖然其鍵能很小, 大量長脂肪鏈的相互作用導致穩定係統的出現. 疏水相互作用在穩定生物聚合物的構象和生物膜的形成中發揮作用.
蛋白質受體分子中的氨基酸殘基含有極性和非極性基團, 決定它們與藥物之間極性和非極性鍵的形成. 極性基團 (-哦, -NH, 首席運營官-, -ñ3H, =O) 提供教育, 主要, 離子鍵和氫鍵. 非極性基團 (氫, 甲基, 環狀自由基等) 與低分子量藥物形成疏水鍵.
從而, 藥物與特定受體的相互作用可以通過各種化學鍵進行, 實力不平等. 所以, 具有靜電膽鹼能受體的類箭毒物質的近似強度 (離子型) 交互作用相當於 5 千卡/摩爾, 離子偶極子 - 2-5 千卡/摩爾, 偶極子-偶極子- 1-3 千卡/摩爾, 氫鍵- 2-5 千卡/摩爾, 范德華連接 - 0,5 千卡/摩爾, 疏水鍵- 0,7 每CH千卡2-團體. 作為靜電相互作用原子間距離的函數,鍵強度的降低為 r-2, 離子偶極子-r-3, 偶極子-偶極子 - r-4, 氫鍵-r-4, 范德華債券 - r-7. 這些類型的連接可能會被中斷, 確保藥物作用的可逆性. 共價鍵更強, 提供物質的長期且通常不可逆轉的影響, 例如:, 烷化抗癌藥. 大多數藥物與受體可逆結合. 其中, 平時, 連接的性質非常複雜: 它可以同時涉及離子, 偶極-偶極, 范德華, 疏水鍵和其他類型的鍵, 這很大程度上是由物質和受體的互補性決定的, 分別, 他們彼此的親密程度.
物質與受體結合的強度稱為“親和力”. 物質, 作用於相同的受體, 可能對他們有不同程度的親和力. 在這種情況下,具有較高親和力的物質可以取代具有較低親和力的物質與受體的連接. 確定“佔據”受體之間的平衡狀態 (DR), 游離受體和游離物質 (丁) 使用解離常數 (ķ丁), 由以下公式確定:
ķ丁=[丁]*[右]/[ DR]
K 的負對數丁 (受體丁) 是親和力的指標. pD指標常用於表徵親和力2, Ť. 它是. EC 的負對數50, (物質濃度, 它產生效果, 形成 50% 從最大效果).
化學相互作用鍵的多樣性及其不等強度, 或者配體和生物受體之間的親和力可以通過藥物的複雜結構來解釋, 含有不同反應性的自由基並具有多維體積形狀, 以及交互過程的複雜性, 往往分幾個階段發生 (階段): 藥物受體複合物的形成; 分子內成團; 複合物的解離.
從而, 藥理作用只能由對生物受體具有明顯親和力的物質引起. 作用的嚴重程度取決於藥物的濃度和受體總數.
如果物質有足夠的內部活性, 那麼它們被稱為激動劑. 內在活性是指激動劑通過改變受體構象而引起生物效應的能力, Ť. 它是. 配體激活受體的能力. 這種現像被認為是激動劑-受體複合物對傳感器的親和力, 將外部信號轉換為內部信號的過程稱為轉導. 細胞內信號傳輸是這些過程的基礎, 就像肌肉纖維的收縮一樣, 細胞分裂, 增殖, 差異化等. 它現在確立, 許多物質怎麼樣 (荷爾蒙, 生物活性肽, 核苷酸, 類固醇, 低分子量生物調節劑等) 細胞有特定的受體. 由於這些物質與這些特定受體相互作用,形成了第二信使 (中介人), 引發一系列生化反應.
有一個概念“部分激動劑» - 藥用物質, 該, 與受體結合, 沒有發揮最大效果. 這種令人費解的現象可能是用不完整的解釋 (在) 藥物-受體複合物的親和力對傳感器的依賴性. 例如, 部分阿片受體激動劑納洛啡的作用與完全阿片受體激動劑嗎啡相似, 雖然比上一個弱. 同時,當一起使用時,納洛啡會減弱或消除嗎啡的作用; 特別是, 嗎啡對呼吸的抑製作用被消除. 異丙腎上腺素是真正的激動劑, 普那特羅是 β-腎上腺素能受體的部分激動劑. 根據受體理論, 真正的激動劑可以引起最大反應, 即使它只與部分受體相互作用.
特定受體可能具有相同或不同的激動劑和拮抗劑結合位點. 不同激動劑可能有不同的結合位點. 在這種情況下, 當激動劑和拮抗劑具有相同的結合位點並且通過增加激動劑的濃度完全消除拮抗劑對受體的阻斷作用時 (達到最大的激動效果), 拮抗劑和激動劑之間的關係稱為競爭性拮抗作用. 如果激動劑和拮抗劑的結合位點不同, 那麼它們之間的關係定義為非競爭性對抗關係. pA 指標常用於表徵拮抗劑2 (拮抗劑摩爾濃度的負對數, 為了獲得激動劑的標準效果,其濃度必須加倍).
在整個生物體的情況下,激動劑和拮抗劑引起某些生理功能的變化. 在這種情況下,拮抗劑的作用由下式決定:, 它們干擾相應天然配體對特定受體的影響 (例如:, M-膽鹼能受體拮抗劑阿托品干擾其激動劑乙酰膽鹼的作用). 變化, 與物質與特定受體的相互作用直接相關, 由術語“主要藥理反應”表示, 這可能是一系列反應的開始, 導致某些生理功能的刺激或抑制”.
器官或系統功能的變化 (例如:, 心臟收縮的強度和頻率的變化, 內臟平滑肌張力, 腺體分泌物, BP和其他人。), 藥物引起的, 表示為 該物質的藥理作用. 所以, 對於強心苷,主要藥理反應是抑制Na+轉運活性, K-ATF-或纖維心肌, 被認為是強心苷可能的特異性受體. 在這方面,K+進入肌纖維和Na+從纖維中排出被破壞。, 細胞質中Ca2+含量增加, 促進肌動蛋白和肌球蛋白的相互作用. 這些變化的結果是心臟收縮的強度增加, 強心苷的主要藥理作用是什麼.
激動劑對特定受體的長期作用常常伴隨著其敏感性的降低. 後者可能與受體的變化有關, 減少他們的數量 (密度) 或流程中斷, 跟隨受體的刺激. 與此同時,激動劑的藥理作用變得不那麼明顯.
從而, 大多數藥物的藥理作用與其對相應特定受體的作用有關.
與生物受體親和力高、內部活性低的物質稱為拮抗劑, 或阻滯劑, 因為他們, 不會引起生物受體構象的變化, 防止內源性和/或外源性激動劑配體與其相互作用. 還有所謂的“次要或沉默受體”, 藥物與其結合, 但沒有藥理作用. 這種“沉默”受體最常存在於蛋白質和血漿中 (但也可以在組織中找到). 與“沉默”受體的連接導致游離藥物濃度降低, 從而降低治療效果.
眾多現代理論, 解釋配體-受體相互作用的機制, 受體本身的狀態, 佔據的受體數量與最終反應之間缺乏比例, 信號傳遞效率的變化以及儲備受體和部分激動劑的存在等。. D. 形成了有關各組藥物代表的作用機制的想法的基礎. 這些相互作用分為受體相互作用和化學相互作用.
藥物與生物受體相互作用的機制 可以如下圖所示: 每個配體 (藥物或生理底物) 與特定受體上的特定位點結合. 激活的受體直接或間接調節離子通量 (1) 和/或其他細胞內過程 (分泌或肌肉收縮) 或激活鳥嘌呤核苷酸結合蛋白系統 (G蛋白), 什麼, 反過來, 增強第二信使酶系統的激活. 幾種不同的第二信使在細胞質中發揮作用, 激活各種靶蛋白, 例如蛋白質- 激酶. 後者作用於特定底物並介導藥理作用.
從所提供的描述中可以清楚地看出, 藥物的作用通過以下機制發生:
- 組織的生理功能 (例如:, 收縮的, 分泌的) 可以被多種受體調節, 因此, 和各種配體;
- 藥物-受體相互作用和組織或器官反應之間可能存在幾個中間步驟, 特別是受體相關第二信使系統的激活;
- 機制效率, 負責刺激-反應序列, 並且受體密度可能因組織而異.
有些藥物的治療作用是由於其直接作用 (與特定受體無關) 與內源性化合物的化學相互作用或其他相互作用機制 (滲透壓, 吸附). 因此對於滲透性利尿劑 - 甘露醇, 尿素 - 沒有特定的受體. 這些物質會增加腎小管的滲透壓, 結果,水的重吸收受到損害,利尿作用增加. 吸附物質的作用與特定受體無關, 酸形成利尿劑.
抗酸藥 (例如:, 氫氧化鋁或氫氧化鎂) 與鹽酸反應生成弱酸性產物. 螯合劑, 與某些金屬粘合, 形成不活潑的化學絡合物.
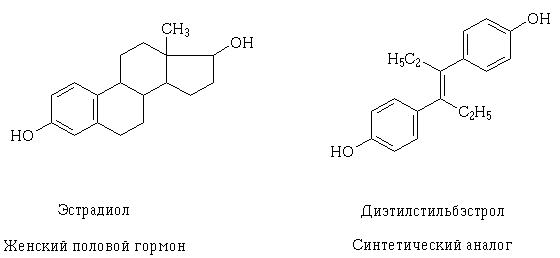
隨著對受體結構和細胞水平上藥物可能的藥效相互作用機制的了解不斷加深,它們的靶向創造已成為可能, 以及解釋, 為什麼藥材能有類似的功效呢?, 不同的, 乍一看, 它的結構. 這種現象的一個例子是雌二醇和己烯雌酚的反式異構體,後者是女性性激素的合成類似物。. 它們的結構分子不同, 但含有相同性質和大小的羥基官能團, 空間位置和方向相似, 由於這些物質的分子可以與相同的受體相互作用並具有相似的藥理作用.
方法, 藥物通過哪些物質產生一定的藥理作用, 由術語“作用機制”表示. 這個概念用於解釋藥物對分子的作用。, 器官和系統水平. 例如, 抗膽鹼酯酶藥物的作用機制在分子水平上歸結為通過與其陰離子和酯酶中心相互作用而阻斷乙酰膽鹼酯酶. 同時, 解釋抗膽鹼酯酶藥物的降血壓作用機制, 表明心動過緩和血管舒張是造成這種效應的原因, Ť. 它是. 在器官水平上考慮這種效應的機制.
藥物作用機制的研究正在進行中, 此外,隨著新數據的獲得,有關特定藥物作用機制的想法不僅可以變得更加詳細, 但也發生顯著變化.
