Studi tentang pembekuan darah
Metode investigasi dari sistem pembekuan darah termasuk kelompok berikut:
- indikatif (umum), memberikan gambaran tentang keadaan seluruh kaskade koagulasi secara keseluruhan dan tahap individu (pendaftaran dapat dibuat secara visual atau dengan perangkat individu - koagulografa, Thromboelastography et al.);
- membedakan defisit faktor individu - tes koreksi koagulasi, tes pencampuran plasma darah yang diteliti dengan plasma darah pasien yang diketahui kekurangan faktor tertentu;
- kuantisasi komponen individu pada aktivitas fungsional mereka dari sistem (tes koagulasi, Studi dan substrat kromogenik lainnya) dan (atau) dengan penanda imunologis;
- mendeteksi aktivasi pembekuan darah intravaskular dan fibrinolisis atas dasar fungsional atau penanda molekuler aktivasi tersebut - untuk mendeteksi beredar faktor koagulasi diaktifkan, produk trombosit degranulasi, komponen pemisahan sistem pembekuan darah atau metabolit daripadanya, munculnya penanda antigen baru faktor diaktifkan dan kompleks mereka, dipercepat metabolization berlabel komponen dari sistem pembekuan darah (mengurangi periode paruh mereka dalam sirkulasi).
Demikian, dalam penilaian pembekuan darah digunakan dengan benar prosedur koagulasi (laboratorium dan instrumental), membentuk dasar dari proses diagnostik, dan imunologis, radionuklida dan jenis penelitian lainnya. Selain itu, dalam banyak kasus, komponen sistem dapat ditentukan berdasarkan aktivitas fungsional, dan imunologis - isi antigen yang relevan dalam darah. Concurrent penggunaan teknik tersebut memungkinkan untuk membedakan bentuk patologi, terkait dengan tidak adanya sintesis faktor pembekuan yang tepat (dalam hal ini sama seperti yang diturunkan aktivitas fungsional, dan jumlah antigen), dan bentuk, di mana molekul faktor disintesis, tapi itu tidak normal dan fungsional cacat.
Untuk menunjukkan bentuk dari faktor pertama sesuai dengan nomor ditambahkan ke tanda "-" (misalnya, VIII, IX- dan t. d.), dan yang kedua - tanda "+". (misalnya, VIII+, IX+).
Perkiraan (umum) tes koagulasi
Penentuan waktu pembekuan darah
Penentuan waktu pembekuan darah (lebih disukai daripada teknik Lee-White) - sudah lama digunakan, cepat diterapkan (di samping tempat tidur) tes indikatif, memungkinkan untuk mengidentifikasi gangguan perdarahan yang signifikan, terkait dengan defisiensi faktor pembekuan darah (kecuali Factor VII) atau aksi antikoagulan dan fibrinolitik. Ini digunakan sebagai panduan untuk tes dan kontrol terapi heparin, penghapusan heparin protamin sulfat. Tes sensitivitas relatif rendah, parameter yang rusak hanya ketika ditandai penurunan faktor koagulasi plasma (di bawah 4-5 %), sehubungan dengan apa yang cocok untuk mendeteksi hemofilia A dan B ringan, serta gangguan koagulasi di angiohemophilia, kekurangan Factor XI, prekallikrein, dan tinggi kininogen berat molekul. Untuk alasan ini, tes tidak dapat digunakan untuk evaluasi pra operasi pasien: di bawah kinerja tes normal (5-10 min) Anda mungkin mengalami perdarahan pasca operasi berlimpah.
recalcification plasma
plasma waktu recalcification - non-standar uji sensitivitas rendah, kurang dapat diandalkan untuk mendeteksi hipokoagulasi, daripada waktu pembekuan darah utuh. Tidak dapat direkomendasikan untuk mendiagnosis gangguan hemostasis.
Waktu tromboplastin parsial plasma teraktivasi
Waktu tromboplastin parsial plasma teraktivasi (APTV, uji kaolin-kephalin) - metode yang sangat sensitif, mendeteksi pelanggaran pembekuan ketika memulai mekanisme internal dari proses. Selektif sensitif terhadap defisiensi faktor koagulasi plasma (sebagai kekurangan trombosit dan faktor 3 platelet kompensasi sefalin diinput eksternal atau eritrofosfatidom).
Ini digunakan untuk memantau heparin yang, pemeriksaan pasien sebelum operasi, dll.. d. Indikator standar bergantung pada sampel sefalin yang digunakan, dalam banyak kasus adalah 37-50 detik (optimal - 37-45 detik).
Kaolin waktu plasma
Kaolin waktu plasma - uji, mirip dengan sebelumnya, tetapi tanpa menambah kephaline plasma (eritrofosfatida), akibatnya, ia sensitif tidak hanya terhadap defisiensi faktor koagulasi plasma, tetapi juga karena kekurangan trombosit dan faktornya 3 Trombosit. Perkiraan evaluasi aktivitas faktor ini dapat dilakukan dengan membandingkan waktu kaolin plasma diselidiki dengan kandungan tinggi dan rendah trombosit (norma - 57-70 dengan).
Penggunaan komponen fosfolipid tidak dianjurkan, memberikan APTT waktu pembekuan sama dengan 55 s atau lebih, karena hal ini secara drastis mengurangi keakuratan dan reproduktifitas pengujian, termasuk dalam penentuan kuantitatif faktor VIII dan IX.
Waktu Plasma Silikon
Waktu plasma silikon adalah waktu rekalsifikasi plasma, diperoleh dengan silikonisasi jarum, tabung reaksi, pipet, t. Ini adalah. dengan aktivasi kontak minimal. Tes ini sensitif terhadap hiperkoagulasi—aktivasi intravaskular dari fase kontak pemicu (faktor XII dan XI), Namun, pelanggaran ini terungkap lebih jelas dengan mendefinisikan waktu pembekuan silikon dari seluruh darah (berdasarkan metode Lee-Putih atau proses pendaftaran tromboelastograficheskoy di kuvet siliconized).
indikator standar tergantung pada silikon dan ditentukan dengan memeriksa darah orang sehat untuk setiap sampel secara terpisah. Ketika memilih silikon adalah yang terbaik, yang paling memperpanjang waktu pembekuan (plasma).
protrombin (tromboplastin) waktu plasma
protrombin (tromboplastin) waktu plasma (waktu cepat, Indeks protrombin) Ini mencirikan tingkat plasma recalcified pembekuan ketika memulai mekanisme eksternal dari proses, t. Ini adalah. menambahkan otak manusia tromboplastin (atau kelinci).
Aktivitas tromboplastin distandarisasi pada sampel campuran normal (kontrol) plasma. Tromboplastin dengan aktivitas 12-18 detik paling sering digunakan. (dalam metode Cepat klasik - 12-13 detik). Semakin lemah tromboplastinnya, semakin besar kesalahan metodenya.
Dalam protrombin yang normal uji waktu plasma mengungkapkan kekurangan terisolasi atau gabungan dari faktor-faktor kompleks protrombin - VII, X, V dan II, dari yang tiga faktor (VII, X kegembiraan) K-vitaminozavisimy dan aktivitas mereka menurun di bawah pengaruh antikoagulan tidak langsung. Dalam hal ini, tes protrombin adalah fundamental dalam mengendalikan kumarin dosis (neodikumarin, atau pelentan, sinkumar et al.) dan obat lain dalam kelompok ini (fenilin).
Waktu protrombin tetap normal dengan kekurangan faktor mekanisme internal aktivasi protrombinase - faktor XII, XI, IX, VIII (t. Ini adalah. untuk semua jenis hemofilia dan cacat Hageman), serta kekurangan prekallikrein dan kininogen berat molekul tinggi (VM kininogen)
Dalam literatur yang berbeda hasil tes protrombin penunjukan. Yang paling tepat adalah menunjukkan waktu tes protrombin dan mengontrol plasma darah dalam hitungan detik (yang juga memberikan informasi tentang aktivitas tromboplastin yang digunakan). Terkadang rasio kedua besaran ini digunakan, t. Ini adalah. indeks (PT dari plasma uji, dari ,)/(PT plasma kontrol, dari), (norma 0.9-1.1).
Bentuk lain dari penilaian indikator ini, yang paling banyak digunakan di laboratorium, adalah perhitungan indeks protrombin sebagai persentase dengan menyusun proporsi aritmatika terbalik (norma - 90-110%), Namun perhitungan ini salah, karena ada hubungan non-aritmatika antara konsentrasi faktor pembekuan dan waktu pembekuan, dan ketergantungan logaritmik. Selain, tes protrombin hanya sensitif terhadap penurunan faktor koagulasi di bawah ini 50 % ukuran normal mereka. Oleh karena itu, disarankan untuk menggunakan penentuan indeks protrombin sebagai persentase menurut kurva pengenceran (1:2, 1:4, 1:8 dan t. d.) sampel plasma normal campuran. Kurva ini dibuat satu kali untuk tromboplastin dengan aktivitas awal yang berbeda. (dari 12 untuk 18 dari) dan digunakan untuk menentukan indeks protrombin pada pasien yang diteliti. Keuntungan dari teknik ini juga, itu hasil dari semua penelitian, termasuk yang dilakukan secara dinamis pada hari yang berbeda, tidak berhubungan dengan sampel plasma darah normal yang berbeda secara acak, dan ke rata-rata parameter standar yang sama, sebagai hasilnya, kesalahan metode ini berkurang secara signifikan. Indeks, diperoleh dari kurva proporsi dan pengenceran plasma normal, sama sekali tidak konsisten satu sama lain. Hal ini juga harus diperhitungkan ketika memantau efek antikoagulan tidak langsung., karena penurunan indeks biasa menjadi 50 % kira-kira setara dengan penurunan indeks sepanjang kurva pengenceran menjadi 25-30%• Dalam hal ini, analisis harus selalu menunjukkan, Bagaimana indeks protrombin dihitung?, apa indikator standar tromboplastin dari aktivitas ini.
Waktu trombin plasma
Waktu trombin plasma, t. Ini adalah. waktu pembekuan plasma sitrat ketika trombin dengan aktivitas standar ditambahkan ke dalamnya, adalah tes utama untuk menilai tahap akhir pembekuan darah. Mempertimbangkan indikator ini penting untuk interpretasi yang benar dari semua tes koagulasi lainnya, karena pelanggaran tahap akhir pembekuan darah pasti akan menyebabkan peningkatan waktu pembekuan pada semua metode di atas.
Dalam kebanyakan kasus, saat melakukan tes trombin, konsentrasi larutan trombin ini digunakan, yang bila dicampur dengan plasma darah dengan volume yang sama, menghasilkan koagulasi dalam 12– 18 dari, tetapi ketika mengenali disfibrinogenemia, konsentrasi yang lebih lemah juga digunakan (menyebabkan koagulasi dalam 30-35 detik).
Waktu trombin - indikator diagnostik penting, pelanggarannya diamati seperti bawaan, dan dengan sering terjadi didapat (sekunder) hipoprotrombinemia, dengan sebagian besar disfibrinogenemia, dan juga di bawah pengaruh heparin, produk fibrinolisis (PDF) dan sejumlah antitrombin lain dan penghambat perakitan monomer fibrin sendiri. Karena itu, waktu trombin di tempat pertama dan lebih terganggu oleh DIC akut dan subakut, yang memainkan peran penting dalam diagnosis yang cepat patologi ini.
Tes autokoagulasi
Tes autokoagulasi (BERTINDAK) - dua tahap yang sangat sensitif, mencirikan proses pembekuan darah ketika dipicu oleh mekanisme internal. Sama seperti APTV, tes ini tidak sensitif terhadap defisiensi faktor VII, tetapi pada saat yang sama indikasinya tidak bergantung pada kandungan fibrinogen (faktor I) dalam plasma darah yang diteliti, bagaimana hal itu berbeda dari semua sampel lain menunjukkan koagulasi.
Keuntungan lain adalah bahwa ACP, bahwa darah diencerkan diselidiki, sehingga secara signifikan meningkatkan sensitivitas untuk kekurangan faktor pembekuan dan, Selain, pelaksanaan ACP tidak memerlukan penggunaan kaolin dan kephaline, sejak standarisasi kontak dan mengaktifkan fosfolipid hemolisate sendiri sel darah merah dicapai itu diselidiki.
Esensi dari ACT adalah, bahwa untuk 2 ml larutan hipotonik (0,222 %) kalsium klorida ditambahkan 0,1 ml darah subjek.
Dalam campuran hemolisat-kalsium ini, protrombinase dan trombin terbentuk, yang aktivitasnya ditentukan oleh penjumlahan berurutan 0,2 ml campuran ini ke 0,2 ml plasma subjek (setiap 2 menit selama yang pertama 10 m, dan kemudian setiap 10 menit untuk 1 tidak).
Plasma subjek merupakan sumber fibrinogen, di mana aktivitas trombin yang terbentuk dalam campuran diuji. Seperti yang ditunjukkan oleh banyak penelitian, bisa diganti dengan plasma darah orang sehat atau larutan fibrinogen. Dalam hal ini, konsumsi darah pasien berkurang menjadi 0,1-0,2 ml (bisa diambil dari jari!), apa mengubah uji autokoagulasi menjadi uji mikrokoagulasi (TIK) dan membuatnya sangat nyaman untuk digunakan dalam pediatri, termasuk saat mempelajari hemostasis pada bayi baru lahir.
Aktivitas koagulasi di ACT dan MCT awalnya meningkat dan pada orang sehat biasanya mencapai maksimal pada menit ke-10, inkubasi campuran darah-kalsium (KCS), ketika koagulasi plasma substrat terjadi dalam 10±1 detik. Kemudian aktivitas koagulasi CCS mulai menurun, yang menunjukkan inaktivasi trombin yang terbentuk di dalamnya. Untuk hemofilia, paparan heparin dan gangguan koagulasi lainnya, aktivitas koagulasi CCS berkurang tajam, dan pergerakan maksimal dari menit ke 10 ke tanggal berikutnya. Dengan hiperkoagulasi, terjadi peningkatan aktivitas trombin yang lebih awal dan lebih signifikan di CCS.
Saat melakukan pengujian dalam satu tabung (penentuannya hanya pada menit ke 10 inkubasi CCS) dapat digunakan untuk memantau terapi heparin. Keuntungan teknik ini dibandingkan uji waktu tromboplastin parsial teraktivasi adalah, bahwa itu menetralkan pengaruh yang tidak seimbang dari sefalin yang berbeda pada waktu pembekuan heparin.
Berdasarkan ACT (TIK) metode sederhana dan akurat untuk diagnosis banding hemofilia telah dikembangkan.
Menggunakan tabel konversi yang diberikan dalam buku referensi, pembacaan ACT (TIK) dapat dinyatakan sebagai persentase dan digambarkan sebagai grafik - autocoagulogram.
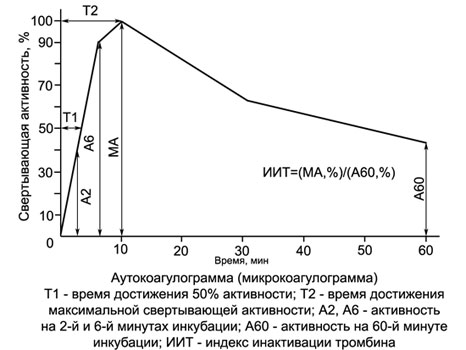
Metode penelitian instrumental juga banyak digunakan untuk menilai sejumlah parameter umum pembekuan darah., terutama menggunakan berbagai koagulograf dan tromboelastograf.
Tromboelastografi tidak hanya memberikan ide dari parameter waktu pembekuan darah atau plasma, tetapi juga pada struktur dan sifat mekanik dari gumpalan terbentuk. Dalam beberapa tahun terakhir, perangkat keras dan metode pendaftaran diperkenalkan standarisasi dan fosfolipid aktivasi kontak dari koagulasi. Koagulasi juga diciptakan untuk pelaksanaan massa tes koagulasi umum - aPTT, protrombin, trombin dan merekam otomatis lainnya dari hasil.
Metode untuk membedakan defisiensi berbagai faktor koagulasi dan kuantifikasinya
Data pada tabel di bawah ini menunjukkan, bahwa studi indikatif pembekuan darah menggunakan tiga tes utama memungkinkan diferensiasi kelompok dari defisiensi berbagai faktor hemokoagulasi plasma. Jadi, perlambatan koagulasi hanya pada tes protrombin (Pelanggaran tipe I) dengan pembacaan normal untuk semua orang lain, ini merupakan karakteristik dari defisiensi faktor VII yang diturunkan atau penurunan tingkat faktor ini pada tahap awal perkembangan penyakit kuning obstruktif atau dalam 1-2 hari pertama pengobatan dengan antikoagulan tidak langsung, ketika penekanan sintesis faktor VII maju dalam perkembangannya, penurunan tingkat semua faktor koagulasi yang bergantung pada vitamin K lainnya.
| Jenis pelanggaran tes koagulasi utama dengan defisiensi faktor koagulasi plasma tertentu | ||||
| Jenis pelanggaran | Faktor kekurangan dalam plasma darah yang diteliti | Tes koagulasi | ||
| APTV, BERTINDAK | PV | televisi | ||
| Saya | VII | – | + | – |
| II | XII | + | – | – |
| XI | + | – | – | |
| IX | + | – | – | |
| VIII | + | – | – | |
| faktor von Willebrand | + | – | – | |
| Prekalikrein plasma | + | – | – | |
| VM kininogen | + | – | – | |
| AKU AKU AKU | II | + | + | – |
| V | + | + | – | |
| X | + | + | – | |
| VII | – | + | – | |
| IX | + | – | – | |
| Saya | + | + | + | |
| XIII | – | – | – | |
| IV | Antikoagulan langsung (Heparin, heparinoid, dll.) | + | + | + |
| Antikoagulan tidak langsung (kumarinы) | + | + | – | |
| Catatan. (+) - memperlambat koagulasi; (-) - tidak ada gangguan pembekuan. | ||||
Gangguan pada mekanisme koagulasi internal saja, t. Ini adalah. waktu tromboplastin parsial teraktivasi dan ACT (Tipe II), diamati dengan defisiensi faktor XII, XI, IX, VIII, Villeʙranda (tidak dalam semua bentuk), prekallikreina dan VM kininogena. Dari jumlah tersebut, pada defek koagulasi herediter, defisiensi faktor XII, prekallikrein dan VM kininogen sangat jarang diamati dan tidak disertai perdarahan apa pun, sedangkan defisiensi faktor VIII (hemofilia A), IX (Hemofilia B) dan faktor von Willebrand sangat umum (lebih besar dari 96 % semua koagulopati herediter) dan disertai pendarahan hebat. Di antara mereka, pertama-tama, diagnosis banding lebih lanjut dilakukan..
Defisiensi faktor XI relatif jarang (sekitar 0,5-1,0 % semua hemofilia), terjadi dengan pendarahan yang sangat ringan (terutama setelah cedera dan operasi) dan menempati tempat perantara antara subkelompok pertama kelainan tanpa gejala dan hemofilia serta penyakit von Willebrand.
Jenis kelainan lain ditandai dengan perpanjangan waktu tromboplastin parsial dan ACT, dan waktu protrombin. Hal ini merupakan ciri dari defisiensi faktor V, X atau II atau dengan defisiensi kompleks semua faktor yang bergantung pada vitamin K (VII, X, IX, II), apa yang diamati pada penyakit kuning obstruktif dan jenis kekurangan vitamin K lainnya, dan juga saat mengonsumsi antikoagulan tidak langsung.
Akhirnya, seperti yang dapat dilihat dari tabel yang sama, Kemungkinan pelanggaran ketiga tes (Tipe IV), apa yang diamati pada hipo herediter dan didapat- dan disfibrinogenemia (tidak semua orang), saat mengonsumsi antikoagulan langsung (geparina, heparinoid, Girudin dan lain-lain.), pengobatan dengan aktivator fibrinolisis dan obat defibrinasi (streptokinase, urokinase, dll.), munculnya antitrombin dan zat patologis dalam darah, mencegah koneksi (perakitan) monomer fibrin - paraprotein, krioglobulin, kompleks imun, serta untuk gangguan perdarahan kompleks, disebabkan oleh sindrom DIC. Dalam hal ini, waktu trombin sering kali terganggu lebih parah dan lebih awal, daripada tes lainnya.
Mempertimbangkan durasi penyakit dan kemungkinan asal usulnya yang turun-temurun atau hubungan sekunder dengan jenis patologi lain dan obat-obatan atau pengaruh lainnya, ada tidaknya perdarahan dan jenisnya, adalah mungkin untuk menentukan dengan tepat asal usul gangguan pembekuan darah yang mendalam ini.
Semuanya uji diferensiasi didasarkan pada prinsip koreksi, t. Ini adalah. pada definisi, sejauh mana kelainan perdarahan yang teridentifikasi diperbaiki atau, sebaliknya, tidak dihilangkan dengan sampel plasma darah atau produk darah yang diperoleh secara artifisial dengan defisiensi faktor koagulasi tertentu yang diketahui.
Untuk tujuan ini, laboratorium khusus membuat sendiri kumpulan plasma darah yang kekurangan faktor, menerimanya dari pasien dengan penyakit mendalam yang diketahui (kurang 1 %) kekurangan masing-masing faktor dan menyimpannya dalam kemasan kecil (oleh 0,5 ml) pada suhu - 30 ° C. Jika perlu, sampel ini dicairkan dan digunakan dalam tes diagnostik..
Plasma, tidak sengaja mencairkannya atau tidak digunakan, tidak dapat dibekukan kembali. Dalam tes koreksi, plasma dengan inhibitor imun dari faktor tertentu tidak boleh digunakan.. Peralatan diagnostik dari sejumlah perusahaan berisi sampel plasma darah beku-kering yang kekurangan faktor koagulasi yang terdeteksi (plasma substrat). Namun, banyak kelainan perdarahan yang sangat jarang terjadi dalam praktik klinis., dalam hal ini, komponen darah normal yang dibuat secara artifisial dengan kekurangan faktor koagulasi tertentu digunakan, serta plasma heterogen (ayam, bebek, dll.).
Tabel tersebut memberikan informasi tentang kandungan faktor pembekuan darah dalam komponen darah, digunakan untuk tes koagulasi korektif tergantung pada umur simpannya. Menggunakan tabel ini, mudah untuk menguraikan pembacaan salah satu dari tiga tes koagulasi utama. Dalam metode pemasyarakatan semacam ini, tes digunakan, terstandarisasi untuk aktivasi kontak dan fosfolipid, t. Ini adalah. kaolin-kephalin atau menggunakan hemolisat (di ACT).
| Kandungan faktor koagulasi dalam plasma darah dengan umur simpan berbeda-beda, digunakan untuk tes korektif | ||
| Plasma darah | Faktor pembekuan | |
| mekanisme internal | mekanisme eksternal | |
| VIII IX XI XII prakalirik | VIIXX II | |
| Warga asli (dengan umur simpan hingga 18 tidak) | ++++ | ++++ |
| Teradsorpsi * | +-++ | –+- |
| Dengan umur simpan lebih dari 24 tidak | -+++ | ++– |
| Dengan umur simpan 2-4 hari (pada suhu +4°C) | Tidak digunakan | ++-+ |
| Tersaring ** | Tidak digunakan | –++ |
| Plasma asli anak ayam atau bebek (sampai umur 3-4 hari) | +++- | Tidak digunakan |
| Catatan. (+) — kehadiran suatu faktor; (-) - ketidakhadiran. | ||
| * Adsorpsi dilakukan dengan barium sulfat dari plasma teroksidasi (kaca4-plasma). atau gel aluminium hidroksida dari plasma sitrat (Al(OH)3-plasma). | ||
| ** Filtrasi dilakukan melalui dua filter asbes (Filter Seitz) - dengan 20 % (penyaring atas) dan 30 % (saringan bawah) kandungan asbes masing-masing meningkat dua kali lipat atau tiga kali lipat 30 dan 20 % filter. | ||
Tes untuk mencampur plasma darah pasien dengan plasma, memiliki kekurangan yang diketahui dari satu atau faktor lain
Tentukan waktu tromboplastin parsial teraktivasi dalam plasma darah uji, plasma biasa (KONTROL) dan dalam plasma yang diketahui mengalami defisiensi faktor VIII (dari pasien penderita hemofilia A), IX (dari pasien penderita hemofilia B), XI dan XII. Campuran kemudian dibuat dari sampel plasma sitrat subjek uji. (7/10 volume) dan berurutan dengan masing-masing plasma yang kekurangan (3/10 volume), dimulai dengan defisiensi faktor VIII dan IX (bentuk patologi yang paling umum!).
Kaolin dan sefalin ditambahkan ke dalam campuran, dan dengan 2 tambang akan melakukan kalsifikasi ulang (pada suhu 37 ° C). Di dalam dia bercampur, di mana waktu tromboplastin parsial teraktivasi tidak menjadi normal, mempunyai kelainan koagulasi yang sama.
Jadi, jika waktu tromboplastin parsial teraktivasi pada pasien yang diperiksa tidak dinormalisasi dengan penambahan plasma darah dari pasien yang diketahui mengalami defisiensi faktor VIII, tetapi dikoreksi oleh plasma darah dari pasien dengan defisiensi faktor IX, dia punya hemofilia A.
Demikian pula,, tetapi berdasarkan tes protrombin, defisiensi faktor kompleks protrombin dapat dibedakan (X, V, VVIVIVIVIVIVIV.).
Tes pembentukan tromboplastin
Untuk membedakan kelainan mekanisme internal pembekuan darah, klasik tes pembentukan tromboplastin dengan penggantian komponen trombosit, persiapannya membutuhkan investasi waktu dan darah yang signifikan, cephalin Kerugian dari tes pembentukan tromboplastin adalah ukurannya yang besar, kebutuhan untuk menyiapkan sejumlah besar reagen, banyak waktu yang dihabiskan untuk implementasinya.
Tes koreksi, berdasarkan uji autokoagulasi.
Tes korektif lainnya sepenuhnya memenuhi tujuan diagnostik cepat., berdasarkan koreksi dengan komponen darah normal yang sama berdasarkan uji autokoagulasi.
Tes ini sangat dapat diandalkan, cepat dan mudah dilakukan dan hanya membutuhkan sedikit (tidak lagi 0,5 ml) jumlah darah subjek, yang memungkinkan penggunaannya dalam praktik pediatrik.
Di dalamnya, seperti pada tes pembentukan tromboplastin, Plasma teradsorpsi dan serum darah lama digunakan untuk koreksi, yang disentrifugasi kembali sebelum penelitian. Tuang ke dalam tiga tabung reaksi 2 ml 0,222 % larutan kalsium klorida dan tambahkan ke dua di antaranya 0,1 ml plasma darah normal yang teradsorpsi (1-Aku adalah tabung reaksi) dan 0,1 ml serum darah normal lama (2-Aku adalah tabung reaksi). Pada tiga tabung reaksi lainnya tambahkan 0,2 ml plasma sitrat normal. Kemudian masukkan setiap tabung reaksi yang berisi larutan kalsium klorida. 0,1 ml darah sitrat subjek.
Tepatnya di 4 menit inkubasi campuran ini, aktivitas pembekuannya diuji pada plasma normal.
Penurunan tajam aktivitas koagulasi hanya pada tabung reaksi pertama (dengan BaSO biasa4-plasma) menunjukkan bahwa pasien mengalami defisiensi faktor IX (Hemofilia B), hanya di tabung reaksi kedua (dengan serum lama) — tentang defisiensi faktor VIII (hemofilia A); jika koreksi terjadi pada kedua tabung reaksi (sama kuatnya), kemudian, jelas, ada kekurangan faktor XI atau XII (cm. Meja. 14).
| Tes koagulasi, membedakan gangguan pembekuan darah berdasarkan mekanisme internal (dengan waktu protrombin dan trombin normal) | |||
| Faktor kekurangan dalam plasma darah yang diteliti | Komponen darah normal, ditambahkan ke plasma uji | ||
| Plasma teradsorpsi (tanpa faktor IX) | serumnya yang lama (tanpa faktor VIII) | Campuran plasma teradsorpsi dan serum lama | |
| Faktor VIII | + | – | + |
| Faktor IX | – | + | + |
| Faktor XI atau XII | + | + | + |
| Catatan. (+) - normalisasi koagulasi; (-) - kurangnya normalisasi koagulasi. | |||
Tes ini sangat sensitif, karena penelitian dilakukan pada encer 20 kali darah ketika kompensasi faktor 3 hemolisat trombosit. Satu-satunya reagen yang digunakan adalah larutan kalsium klorida hipotonik, apa yang membuat sampel menjadi publik.
Teknik tes koreksi juga sama sederhananya., dilakukan berdasarkan tes protrombin untuk membedakan defisiensi faktor II, V dan VII+, X (di meja).
| Tes koagulasi, дифференцирующие дефицит факторов II, V и VII+, +X, выполняемые на основе протромбинового теста (при нормальном тромбиновом времени) | ||||
| Faktor kekurangan dalam plasma darah yang diteliti | Komponen darah normal, ditambahkan ke plasma uji | |||
| Plasma teradsorpsi (без факторов II, VII, X) | Старая плазма (без фактора V) | Профильтрованная плазма (tanpa faktor 4. X-Proxing adalah sebuah kesederhanaan.) | serumnya yang lama (tanpa faktor II asing oleh V) | |
| Faktor VII atau X | – | + | – | + |
| Faktor V | + | – | + | – |
| Faktor II | – | + | + | – |
| Catatan. (+) - normalisasi koagulasi; (-) - kurangnya normalisasi koagulasi. | ||||
Untuk membedakan defisiensi faktor VII dan faktor X, tes koagulasi tambahan dilakukan dengan penambahan larutan bisa ular viper ke dalam tes plasma darah - obat lebetox (konsentrasi racun seperti itu dipilih, yang dengan adanya sefalin dan kalsium klorida menyebabkan koagulasi dalam 20-25 detik; semua bahan diambil dalam jumlah banyak 0,1 ml dan aduk) (tabel di bawah ini).
Persiapan racun ular berbisa Russell digunakan untuk tujuan yang sama., tinggal di India (persiapan tunjangan).
| Tes koagulasi, membedakan defisiensi faktor VII dan X dengan menggunakan racun ular berbisa (lebetox) | |||
| Faktor kekurangan dalam plasma darah yang diteliti | Tes | ||
| dengan racun ular berbisa + sefalin + kalsium klorida | dengan racun ular berbisa + sefalin + kalsium klorida + plasma darah yang disaring (sumber faktor V a VIII) | protrombin | |
| Faktor X | – | – | – |
| Faktor VII | – | + | + |
| Catatan. (+) - normalisasi koagulasi; (-) - kurangnya normalisasi koagulasi. | |||
Diagnosis banding diselesaikan, jika perlu, dengan penentuan kuantitatif faktor defisiensi atau penghambat imun spesifiknya, Mengapa teknik standar khusus yang sangat sensitif digunakan?. Teknik ini menggunakan konstruksi kurva pengenceran sampel campuran plasma darah normal dengan koreksi defisiensi semua faktor, kecuali yang sedang dipelajari. Kurva ini digunakan untuk menentukan aktivitas faktor uji dalam plasma pasien..
Terutama penting untuk mengukur konsentrasi faktor VIII dan IX, serta adanya inhibitornya pada pasien hemofilia A dan B (terutama sebelum dan selama operasi dan selama terapi penggantian intensif), serta dengan perdarahan postpartum yang banyak dan tertunda, bila perlu untuk membedakan antara sindrom DIC dan patologi yang lebih langka - munculnya penghambat imun faktor VIII (bahkan lebih jarang - faktor V).
Dengan defisiensi faktor XIII yang parah (patologi herediter yang sangat langka) semua tes koagulasi normal, tetapi gumpalan tersebut larut dalam urea 5M atau 7M.
Ini juga membantu untuk membedakan defisiensi berbagai faktor koagulasi dengan mempertimbangkan derajat dan, terutama, waktu normalisasi pembacaan tes setelah pemberian produk darah secara intravena kepada pasien, t. Ini adalah. memperhitungkan koreksi hidup menurut metode L. 3. Barkagan.
Teknik ini sangat efektif bila terdapat perbedaan besar dalam harapan hidup faktor pembeda yang beredar. Jadi, Waktu paruh faktor kompleks protrombin bervariasi dari beberapa jam (faktor VII) hingga beberapa hari (faktor II). Faktor X menempati posisi perantara di antara keduanya (2- 2,5 hari) dan V (12— 18 jam).
Oleh karena itu, setelah transfusi plasma jet besar-besaran, indeks protrombin meningkat dengan defisiensi faktor VII dalam waktu yang sangat singkat, dengan defisiensi faktor V - sedikit lebih lama (kurang lebih 4-6 kali), dan dengan kekurangan faktor X dan, terutama, II untuk jangka waktu yang lebih lama (selama 1-2 hari). Indikasi dalam hal ini adalah pengaruh obat PPSB pada indeks protrombin (konsentrat faktor VII, IX, X kegembiraan). Ini juga menormalkan waktu protrombin dalam jangka pendek jika terjadi defisiensi faktor VII dan lebih lama (berkali-kali!) dengan defisiensi faktor X dan II. Karena obat ini tidak mengandung faktor V, kekurangan ini tidak dapat diperbaiki olehnya.
Perbedaan serupa terungkap selama transfusi dan terapi penggantian faktor mekanisme koagulasi internal (XII, XI, SIV adalah), apa yang dicatat oleh tes tromboplastin parsial teraktivasi.
Yang menarik adalah dinamika koreksi tingkat faktor VIII dan pembacaan aPTT selama terapi transfusi untuk penyakit hemofilia A dan von Willebrand. Pada penyakit pertama, terjadi perbaikan koagulasi secara cepat dan maksimal setelah transfusi. (semprot, cepat!) plasma antihemophilus atau pemberian kriopresipitat, dan kemudian dengan cukup cepat (selama 10-18 jam) penurunannya yang stabil, sedangkan pada penyakit von Willebrand terjadi peningkatan aktivitas koagulasi selama beberapa jam setelah transfusi, dan kemudian penurunannya jauh lebih lambat, dibandingkan dengan. Oleh karena itu, transfusi pengganti lebih jarang digunakan dalam pengobatan penyakit von Willebrand., dibandingkan dengan hemofilia A.
Studi aktivitas fungsional faktor koagulasi dan komponen kalikrein-kinin dan sistem fibrinolitik menggunakan substrat kromogenik
Metode ini didasarkan pada studi tentang aktivitas enzim proteolitik dan inhibitornya, terlibat dalam pembekuan darah, fibrinolisis dan pembentukan kinin, oleh intensitas dan laju pembelahan peptida yang secara khusus sensitif terhadap enzim ini, setelah degradasi, zat pewarna dilepaskan (β-nitroanilin).
Derajat warna campuran yang bereaksi ditentukan secara spektrofotometri, dan berdasarkan intensitasnya, aktivitas enzim yang bersangkutan dinilai (faktor pembekuan, kallickreina, plasmin dan lain-lain.), dan dengan menghambat proses - tentang aktivitas penghambat enzim.
Jadi, misalnya, efek heparin dan antitrombin III dapat dinilai dengan melemahkan pembelahan substrat kromogenik oleh faktor Xa atau trombin, dan aktivitas α2-antiplasmin - dengan melemahkan efek plasmin pada substrat kromogenik yang sesuai. Substrat kromogenik atau memiliki sebutan digital (misalnya, s-2222), atau disebut kromosom dengan awalan disingkat, menunjukkan enzim itu, dimana substrat ini sensitif (misalnya, Chromozym PL adalah substrat plasmin, Chromozym TH — substrat trombin, Chromozym PK — substrat prekallikrein/kallikrein, dll. d.).
Substrat kromogenik memperluas kemungkinan mempelajari sistem hemostasis, namun belum cukup tersedia untuk banyak laboratorium. Beberapa penelitian, dibuat dengan bantuan mereka, tidak memiliki keunggulan dibandingkan uji koagulasi konvensional dan memberikan hasil yang sesuai; dalam kasus lain, penggunaannya menyederhanakan dan mempercepat penelitian, membuatnya lebih akurat; ketiga, metode ini mempunyai arti tersendiri dan tidak dapat digantikan dengan uji koagulasi (misalnya, definisi prekalikrein).
Иммунологическое определение компонентов системы гемостаза
Иммунологическое определение компонентов системы гемостаза выполняется методами:
- Иммунопреципитации;
- Иммуноэлектрофореза;
- Radioimunologi dan lain-lain dengan antisera yang sesuai
Dalam hal ini, kandungan antigen faktor koagulasi tertentu dalam plasma darah dinilai. (atau pecahannya), bukan aktivitas fungsional, yang dapat dikurangi secara tajam dengan kadar antigen normal dalam plasma. Situasi ini umum terjadi pada semua kasus tersebut, ketika zat abnormal disintesis di dalam tubuh (kekurangan secara fungsional) faktor, mempertahankan antigenisitasnya, tetapi kurang kemampuan untuk berpartisipasi dalam hemostasis.
Hal ini memungkinkan untuk membedakan antara penghentian total sintesis faktor-faktor yang sesuai dan pembentukan bentuk anomalinya..
Вместе с тем ряд компонентов системы гемостаза может определяться только иммунологически.
В эту группу входят такие важные исследования, как определение следующих компонентов:
- -tromboglobulin;
- α2-makroglobulin;
- protein C dan S;
- antigen faktor VIII:C dan VIII:Rkopi;
- produk fibrinolisis (PDF);
- neoantigen dari kompleks trombin - antitrombin III dan plasmin - antiplasmin;
- sejumlah tes lainnya.
Oleh karena itu, penelitian imunologi secara signifikan melengkapi penilaian fungsional berbagai bagian sistem hemostatik.
Tes diagnostik, berdasarkan penggunaan obat dari bisa ular sebagai reagen
Sudah lama didirikan, bahwa bisa banyak ular mengandung enzim proteolitik yang sangat aktif, menyebabkan pembekuan darah dan mempengaruhi berbagai bagian kaskade koagulasi. Akibatnya, bisa ular dan koagulase yang diisolasi darinya banyak digunakan untuk mengenali gangguan hemostatik, kuantifikasi faktor pembekuan, deteksi dan kuantifikasi kompleks fibrin-monomer terlarut (RFMK) dan sejumlah penelitian lainnya.
Пробы со змеиными ядами часто намного упрощают и делают более оперативной диагностику нарушений гемостаза.
Tabel tersebut memberikan data tentang mekanisme kerja racun pada sistem pembekuan darah dan kemungkinan penggunaan diagnostik masing-masing racun..
| Гемокоагулирующие свойства змеиных ядов и их использование в диагностической практике | |||
| Наименование змей * и препаратов из их ядов | Механизм действия на свертывающую систему | Отличия от свойств естественных факторов свертывания | Возможности диагностического применения |
| Гюрза Vipera lebetina); lebetox (гадюка Расселла; tunjangan) | Активатор фактора X (в присутствии кальция, фактора V и фосфолипида **) | В отличие от тканевого тромбопластина не содержит фосфолипида и не компенсирует его дефицита. Не нуждается для реализации свертывания в факторе VII | Определение фактора и тромбоцитов и его освобождения при агрегации; разграничение дефицита факторов VII и X; количественное определение фактора X |
| Эфа многочешуйчатая (Echis multisgumatos) и эфа песчаная (Echis carinatus); èkarin, èhitoks | Активатор фактора II, образует атипичный тромбин-Ем | В отличие от α-тромбина, тромбин-Ем не блокируется гепарином и антитромбином III, не активирует фактора XIII (сгустки лизируются в мочевине), коагулирует весь пул фибриногена и все растворимые комплексы фибрин-мономеров | Выявление гиперкоагуляции, в том числе скрытой, при лечении гепарином; количественное определение всего фибриногена и РФМК с целью диагностики тромбинемии и ДВС- sindroma |
| Щитомордник обыкновенный (Aghistrodon halus halus), а также многие гремучие змеи тропической Америки и Азии; анцистрон-Н1, рептилаза, ботропклотаза, кроталаза, анкрод и др. | Свертывает фибриноген, отщепляя только пептиды А и образуя неполные мономеры фибрина (дес-А-фибрин) | Не отщепляет пептиды В, не активирует фактор XIII и тромбоциты, не вызывает ретракцию сгустков, не блокируется гепарином, быстро лизирует сгустки | Распознавание дисфибриногенемий; оценка роли гепарина в нарушении конечного этапа свертывания (в сопоставлении с тромбиновым временем) |
| * Все указанные змеи обитают в Средней Азии (в скобках указаны другие виды со сходным механизмом действия и фирменные препараты из них; гадюка Расселла обитает в Индии, гадюка Дабойа — в Австралии. | |||
| ** Аналог кефалина и тромбоцитарного фактора 3. | |||
Эти возможности еще более расширяются при одновременном использовании нескольких ядов и простейших общих коагуляционных тестов. Jadi, misalnya, одновременное применение коагуляционных проб с ядом гюрзы и эфы позволяет легко дифференцировать дефицит факторов VII, Х-V и II (в таблице ниже), а с дополнительной коррекцией профильтрованной нормальной плазмой (источник факторов V и II) —дефицит факторов X и V.
| Коагуляционные тесты с применением различных ядов, дифференцирующие дефицит факторов протромбинового комплекса | |||
| Faktor kekurangan dalam plasma darah yang diteliti | Tes | ||
| с ядом гюрзы+кефалином | с ядом эфы | protrombin | |
| VII | + | + | – |
| X+V | – | + | – |
| II | – | – | – |
| Catatan. (+) - normalisasi koagulasi; (-)—отсутствие нормализации свертывания. | |||
Определение основных физиологических антикоагулянтов
Наиболее важное значение имеет определение активности основного физиологического антикоагулянта — антитромбина III, снижение которой может быть генетически обусловленным (первичная тромбофилия) либо вторичным вследствие интенсивного потребления (DIC, массивные тромбозы) или ускоренного метаболизма (лечение гепарином, L-аспарагиназой, синтетическими контрацептивными средствами) и блокады иммунными комплексами, парапротеинами, фибронектином, белками острой фазы.
В любом случае снижение активности антитромбина III ниже 60—65 % поддерживает внутрисосудистое свертывание крови, делает менее выраженным антикоагулянтное действие гепарина. Вместе с тем очень часто между уровнем антитромбина III и снижением чувствительности к гепарину нет закономерного соответствия.
При этом обычно ослабление антикоагулянтного действия гепарина существенно преобладает над степенью снижения активности антитромбина III. Terbukti, что при разных формах дефицита антитромбина III сродство его к гепарину может меняться в различной степени. Selain, разные фракции гепарина, соотношение которых в лекарственных средствах весьма изменчиво, также имеют различное сродство к антитромбину III. Поэтому практически важно исследовать как собственно активность антитромбина III, так и его способность превращаться под влиянием гепарина в быстродействующий антикоагулянт.
Антикоагулянтная активность антитромбина III
Антикоагулянтная активность антитромбина III определяется по способности исследуемой плазмы крови (разведенной — метод Копли—Винтерштейна или дефибринированной тепловой денатурацией pada suhu 56 °С — методы Лолигера, Абильдгаарда и др.) инактивировать в течение определенного срока вводимый извне тромбин. Остаточная активность тромбина в такой плазме может определяться по ее свертывающей активности (на фибриногене, адсорбированной сульфатом бария плазме) либо по расщеплению хромогенного субстрата, чувствительного к тромбину или фактору Xa (поскольку антитромбин III инактивирует и этот фактор).
Гепарин-кофакторная активность
Гепарин-кофакторная активность содержащегося в плазме крови антитромбина III длительный период определялась с помощью теста толерантности плазмы к гепарину, который может считаться ориентировочным, поскольку дает очень большой разброс нормальных показателей и недостаточно воспроизводим.
Значительно более точны и воспро изводимы тесты, в которых исследуется влияние различных концентраций гепарина на тромбиновое время исследуемой плазмы, содержащей небольшое количество тромбоцитов. Сравнение проводится с удлинением тромбинового времени контрольной нормальной плазмы крови, к которой добавляются те же образцы гепарина.
Jadi, в тромбин-гепариновом тесте к исследуемой плазме крови добавляются такие количества гепарина, которые в контроле удлиняют тромбиновое время с 15 до 32—35 с (малая концентрация) и до 95—110 с (высокая концентрация гепарина). По этим данным рассчитываются индексы активности антитромбинов плазмы (ААП) и антикоагулянтного резерва плазмы (АРП).
Также широко используются сходные методики с оценкой степени инактивации тромбина как в коагуляционных тестах, так и на хромогенных субстратах.
Иммунологическое определение антигена антитромбина III
Иммунологическое определение антигена антитромбина III позволяет дифференцировать различные виды тромбофилии:
- с недостаточным синтезом антитромбина III (уровень антигенного маркера снижен адекватно снижению активности);
- с сохраненным синтезом аномальных и функционально неполноценных его форм (уровень антигенного маркера намного выше, чем активность).
Протеины C и S, тромбомодулин и α2-макроглобулин определяются иммуноэнзиматическими методами.
