المايلوما المتعددة – المايلوما
تنبعث منها المرض ميلومنا نودولوس منتشر النموذج الأكثر شيوعاً, منتشر, أشكال متعددة نودولوس، ونادراً ما ينظر الحشوي.
يتطور الورم النقوي المتعدد في أغلب الأحيان بين سن 45 و65 عامًا., يحدث بتكرار متساوي في كلا الجنسين. هناك تقارير في الأدبيات عن المايلوما العائلية, وكذلك حالات نظيرات بروتينات الدم الحميدة والورم النقوي في نفس العائلة. التحليل الوراثي الخلوي لخلايا المايلوما يمكن أن يكشف عن كمية (اختلال الصيغة الصبغية) والهيكلية (حذف, النقل) التغييرات, التي هي غير محددة للورم النقوي, حيث يتم ملاحظتها أيضًا في الأورام الدموية الأخرى.
قد يستغرق تطور المرض سنوات, وفقًا لمؤلفين مختلفين - من 12 قبل سنة 20 سنة أو أكثر.
الأعراض السريرية للورم النخاعي
ترتبط الأعراض السريرية للمرض ارتباطًا وثيقًا بالتغيرات في الأعضاء والأنظمة المختلفة واضطرابات استقلاب البروتين والمعادن.
يتجلى الضرر الذي يلحق بالهيكل العظمي في الألم, الأورام والكسور. غالبًا ما تتأثر العظام المسطحة والقصيرة (ضلوع, فقرات, مجذاف, عظم القفص الصدري), في كثير من الأحيان - المشاش للعظام الطويلة. ويصاحب تكاثر أنسجة الورم تغيرات مدمرة. غالبًا ما تحدث الكسور في موقع الألم الشديد.. يمكن للأورام على شكل نمو بؤري بأحجام مختلفة أن تبرز خارج الأنسجة العظمية.
عندما يتم ثقبها، يتم العثور على خلايا المايلوما في بعض الأحيان. نتيجة لانحلال عظم المايلوما، يتم تعبئة أملاح الكالسيوم من العظام. ومع ذلك، لفترة طويلة كميتها في دم المرضى ضمن الحدود الطبيعية ويلاحظ فرط كالسيوم الدم فقط في 20-40 % المرضى, بشكل رئيسي في الفترة النهائية للمرض, وخاصة مع آزوتيميا.
مع الراحة الصارمة في الفراش، يعاني المرضى من زيادة في عمليات انحلال العظام., مما يؤدي إلى زيادة حادة في كمية الكالسيوم في الدم. إن انخفاض مستوى الكالسيوم في الدم نتيجة العلاج الوراثي الخلوي يؤكد العلاقة المرضية بين فرط كالسيوم الدم وانحلال عظم المايلوما.
تظهر الأشعة السينية للعظام المصابة عيوبًا, يتوافق في الشكل والحجم مع ورم المايلوما. أكثر ما يميزه هو الأشعة السينية للجمجمة ("جمجمة هولي"), حيث يبدو أن العيوب الدائرية والبيضاوية قد أكلتها العثة أو تم التخلص منها بلكمة. يمكن ملاحظة تغييرات مماثلة مع نقائل الأورام الخبيثة في عظام الجمجمة, وفي الحالات, عندما تنتج التحبيبات المتضخمة من الأم العنكبوتية بؤرًا مستديرة للتطهير على الصور الشعاعية.
سمة من المايلوما المتعددة و تغيرات الأشعة السينية في العمود الفقري في شكل هشاشة العظام البؤرية أو المنتشرة. يتم تسطيح الفقرات, على شكل إسفين أو عدسي, قد يكون على شكل القوس, ويكتسب في النهاية مظهر فقرات السمكة. في الشكل المنتشر من المايلوما، يمكن للأشعة السينية أن تكشف هشاشة العظام المنتشر دون عيوب العظام. الأشعة السينية أشكال سلبية من المايلوما (في حالة عدم وجود أي تغييرات في العظام) تمثل حوالي 10 % جميع حالات المايلوما.
يمكن العثور على ارتشاح الخلايا البلازمية في جميع الأعضاء الداخلية تقريبًا. زيادة الكبد أو الطحال لوحظ في 5-13 % المرضى. ومع ذلك، في نصفهم فقط يكون تضخم هذه الأعضاء والغدد الليمفاوية ناتجًا عن ارتشاح خلايا المايلوما, وفي الوقت نفسه، توجد أيضًا خلايا المايلوما في الدم المحيطي (سرطان الدم في الخلايا البلازمية). وفي حالات أخرى، يحدث تضخم الكبد أو الطحال بسبب الحؤول النقوي مع المايليميا وأحيانًا ظهور خلايا الدم الحمراء في الدم المحيطي.
في بداية المرض، لم يتم الكشف عن أي تغييرات في الدم المحيطي. عدد الكريات البيض ومخطط الكريات البيض طبيعيان أيضًا, على الرغم من أنه في بعض الحالات يمكن ملاحظة قلة العدلات مع كثرة الخلايا اللمفاوية النسبية أو العدلات مع التحول إلى اليسار إلى الخلايا النقوية وحتى الأشكال الأصغر سنًا. عادة ما يرتبط قلة العدلات باستخدام أدوية تثبيط الخلايا. في معظم أشكال المايلوما، غالبًا ما تتم ملاحظة كثرة الوحيدات المطلقة ويتم اكتشاف خلايا البلازما المفردة, باستثناء شكل اللوكيميا, حيث يتم إطلاق خلايا المايلوما بأعداد كبيرة في الدم المحيطي. في معظم الأحيان، يتم تصنيف سرطان الدم في خلايا المايلوما على أنه مرض مزمن., داء البلازما الحاد نادر جدًا. مع تقدم المايلوما، يصاب المرضى بفقر الدم, التسبب فيها ليس واضحا تماما.
الأنيميا, عادة, normohromnaja. لا يتم زيادة عدد الخلايا الشبكية. في بعض الأحيان، مع فقر الدم الشديد، تظهر الخلايا الطبيعية في الدم المحيطي. يتم زيادة ESR في معظم حالات المايلوما, باستثناء المايلوما غير المفرزة, وكذلك المايلوما بنس جونز (أمراض السلسلة الخفيفة), يحدث مع انخفاض مستوى إفراز الغلوبولين المناعي. عدد الصفائح الدموية طبيعي لفترة طويلة, على الرغم من ملاحظة فرط الصفيحات في بعض الأحيان في بداية المرض.
دراسة ثقب نخاع العظم في المايلوما تجعل من الممكن في 90-96 % حالات الكشف عن خلايا المايلوما, والتي تعتمد على مرحلة المرض وشكله (منتشر, منتشر البؤر أو متعدد البؤر) يمكن أن يكون موجودا أو في شكل تسلل موحد, أو, يحدث في كثير من الأحيان, جزر منفصلة في كتلة العناصر النخاعية. يمكن اكتشاف مثل هذه الجزر من خلايا المايلوما في المستحضرات ذات التكبير المجهري المنخفض.
قد تشبه خلايا المايلوما الأرومات البلازمية, الخلايا البروبلاسمية والبلازماتية. السمة الخاصة هي وجود اثنين, ثلاثة- ومع وجود عدد كبير من نوى خلايا المايلوما بأحجام مختلفة.
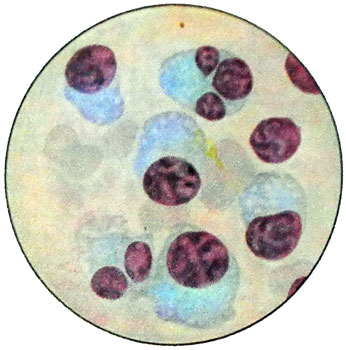
اعتمادا على نوع الخلية السائدة، يتم تمييز الورم الأرومي النخاعي البلازمي, المايلوما-ورم البلازماويات. لقد تم الآن إثبات تكوين وإفراز البروتينات المرضية بواسطة خلايا ورم البلازماويات. يحدث إطلاق الإفرازات في الدم عن طريق الخلايا السرطانية من خلال مسار الهولوكرين., تي. إنها. حسب نوع الغدة وحيدة الخلية.
متلازمة أمراض البروتين في المايلوما يتجلى من خلال فرط بروتينات الدم, الذي يتطور بسبب فرط جلوبيولين الدم.
تنخفض مستويات الألبومين, وبالتالي تنخفض نسبة الألبومين إلى الجلوبيولين إلى 0.6— 0,2. تزداد لزوجة الدم, ويلاحظ تراص تلقائي لخلايا الدم الحمراء على شكل أعمدة معدنية, تفاعلات البروتين الرسوبي الإيجابية, ظاهرة تأخر انحلال الدم في تفاعل واسرمان.
خصائص الجلوبيولين في المايلوما
المعيار الأكثر أهمية وتحديدًا للورم النقوي هو ظهور الغلوبولين المناعي جي, أ, د, قال إي (مع سرطان الدم في خلايا البلازما) أنواع.
تتميز المتغيرات البيوكيميائية التالية للورم النقوي::
- المايلوما G;
- أ- المايلوما;
- د- المايلوما;
- المايلوما الإلكترونية;
- مرض السلسلة الخفيفة (المايلوما الجزيئية بنس جونز);
- المايلوما غير المفرزة;
- المايلوما ديكلون.
نادرا (0,5 % الحالات) يحدث المايلوما.
في مخطط كهربية المصل، يوجد PIg على شكل ضيق, تجويف ملون بشكل مكثف بين γ- وب-, أقل في كثير من الأحيان γ- и ل2-أجزاء الجلوبيولين.
عادةً ما يُطلق على الشريط البروتيني الضيق المدمج الموجود على مخطط كهربية القلب اسم التدرج M.
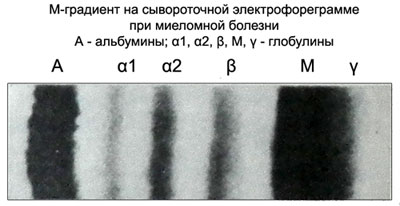
في مخطط البروتين، يبدو التدرج M وكأنه قمة.
فرط غاما غلوبولين الدم التفاعلي (التهاب المفاصل الروماتويدي, تليف الكبد, ورم) على عكس التدرج M في المايلوما، فإنه يبدو وكأنه شريط واسع. في مرض بنس جونز، لا يوجد تدرج M في مخطط بروتين المصل. لا يمكن اكتشاف الخنازير إلا في البول.
بروتين بنس جونز الجزيئي على مخطط كهربية البول يتم تمثيله بشريط ضيق بين γ- и ل2-الجلوبيولين. هذا المؤشر هو علامة مرضية تمامًا لمرض هيموبلاستوز نظير البروتين ويتم اكتشافه في 95 %.
الرحلان الكهربائي لمصل الدم والبول يجعل من الممكن اكتشاف المايلوما 99 % الحالات, باستثناء المايلوما غير المفرزة.
مع نمو الورم، يزداد عدد البروتينات, ولكن تحت تأثير العلاج تثبيط الخلايا فإنه يتناقص, وهو بمثابة مؤشر على فعالية العلاج المطبق.
مظاهر المايلوما المتعددة
الكلية نظيرة البروتينية - المظهر الأكثر شيوعًا للورم النقوي. ثابت, قد تكون البيلة البروتينية المستمرة هي العرض الوحيد للورم النقوي المتعدد, وتختلف شدته على نطاق واسع. حتى مع وجود مستويات كبيرة من بروتينية (إلى 60 % سنجاب) المرضى ليس لديهم تورم, نقص بروتينات الدم, فرط كوليسترول الدم وارتفاع ضغط الدم.
تصلب الكلية الصاعد هو أساس الفشل الكلوي في المايلوما (انكماش الكلى الكلوية), والذي يحدث بسبب إعادة امتصاص بروتين بنس جونز. العوامل الإضافية هي فقدان بروتين بنس جونز في الأنابيب الكلوية مع تطور بؤر التعرق الكلوي داخل الكلى, وكذلك تكلس الكلى, الداء النشواني من سدى بهم, تسلل خلايا البلازما وعدوى المسالك البولية الصاعدة.
تتضمن العملية المرضية الأغشية القاعدية وميزانجيوم الكبيبات الكلوية.
هيالين و (كثير من الأحيان أقل) القوالب الحبيبية والظهارية. في حالات نادرة، قد تحدث بيلة دموية دقيقة. رد فعل قلوية البول, يظهر الفوسفات في البول. لكسور العظام, الالتهاب الرئوي, في المواقف العصيبة، قد يصاب المرضى الذين يعانون من المايلوما المتعددة بفشل كلوي حاد يصل إلى انقطاع البول. في 15 % المرضى لديهم داء نظير النشواني (نظير بروتينات الأنسجة).
يتميز المايلوما بانخفاض كمية الغلوبولين المناعي الطبيعي. ولم يتم بعد توضيح آلية هذه العملية. غالبًا ما يكون نقص غاما غلوبولين الدم مصحوبًا بانخفاض في تكوين الأجسام المضادة, ما يؤثر على حساسية المرضى للعدوى.
أحيانا (في 2-5 % الحالات) في المرضى الذين يعانون من المايلوما عند تبريد المصل أدناه 37 درجة مئوية تترسب البروتينات نظيرة. هذا - الجلوبيولين البردي, البروتينات, وجود خاصية الترسيب أو التجلم عند تبريد مصل اللبن. تظهر في التهاب الشغاف الإنتاني تحت الحاد, التهاب محيط الشريان العقدي, أمراض الكلى المزمنة.
في بعض الأحيان، عند تبريده، تزداد لزوجة الدم دون تكوين راسب مرئي.. وهكذا, يعتمد التشخيص المختبري للورم النقوي المتعدد على اكتشاف خلايا البلازما في نخاع العظم, الكشف عن الغلوبولين المناعي في مصل الدم والبول أو في أحد هذه الوسائط. فقط في وجود الخلايا يمكن للمرء أن يفكر في تشخيص ورم البلازماويات. الفحص بالأشعة السينية إضافي في تشخيص المرض., ومع ذلك، فإن غياب التغيرات العظمية لا يستبعد تشخيص المايلوما, وكذلك البيانات الإشعاعية الإيجابية بدون علم الخلايا ولا يمكن أن تكون بمثابة أساس لتشخيص المايلوما. النخاع الشوكي (المايلوما) في كثير من الأحيان يجب التمييز بينه وبين مرض فالدنستروم.
